Nature重磅:雄激素缺失反而加速脑肿瘤生长——揭开胶质母细胞瘤性别差异新机制
时间:2026-05-08 20:11:36 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
胶质母细胞瘤是最常见且恶性程度最高的原发性脑肿瘤,长期以来医学界观察到一种令人困惑的现象:男性患者的发病率更高、预后更差。尽管此前的研究普遍认为雄激素具有免疫抑制作用,会促进肿瘤进展,但这一理论无法完全解释脑肿瘤中显著的性别差异。随着年龄增长,男性体内血清睾酮水平自然下降,而这一变化与胶质母细胞瘤患者预后之间的关系,一直是肿瘤免疫学领域亟待解决的关键问题。
近日,来自克利夫兰诊所等多个研究机构的科学家首次揭示了雄激素在脑肿瘤中截然不同的“抑瘤”作用。研究团队通过小鼠模型、单细胞测序、空间转录组学以及真实世界患者数据分析,发现雄激素缺失会通过过度激活下丘脑-垂体-肾上腺轴,诱导系统性T细胞功能障碍,从而加速脑肿瘤生长。这一发现颠覆了传统认知,为理解脑肿瘤的性别差异及开发新的治疗策略提供了全新视角。相关成果以“Androgen loss accelerates brain tumour growth via HPA axis activation”为题发表在《Nature 》上。

研究团队首先通过一系列动物实验验证了雄激素对脑肿瘤生长的独特影响。他们将5-6周龄的雄性小鼠进行去势手术(模拟雄激素剥夺),随后颅内植入多种小鼠胶质母细胞瘤模型。结果令人惊讶:与假手术组相比,去势小鼠的生存期显著缩短,肿瘤体积也更大(图1a、b)。这种效应并非肿瘤细胞类型特异性——当研究人员将非胶质母细胞瘤的癌细胞(如膀胱癌MB49细胞或黑色素瘤B16-F10细胞)植入颅内时,去势小鼠同样表现出生存期缩短(图1c)。然而,当同样的胶质母细胞瘤细胞被植入皮下(颅外)时,去势反而延缓了肿瘤生长(图1d)。这种“部位特异性”效应进一步通过药物实验得到证实:使用雄激素受体抑制剂恩杂鲁胺治疗会缩短小鼠生存期,而外源性睾酮补充则能挽救去势导致的生存期缩短(图1e-g)。更为重要的是,对美国SEER数据库中胶质母细胞瘤患者的真实世界数据分析显示,接受睾酮补充联合替莫唑胺治疗的男性患者,中位总生存期从12个月延长至16个月,死亡风险降低38%(图1i)。
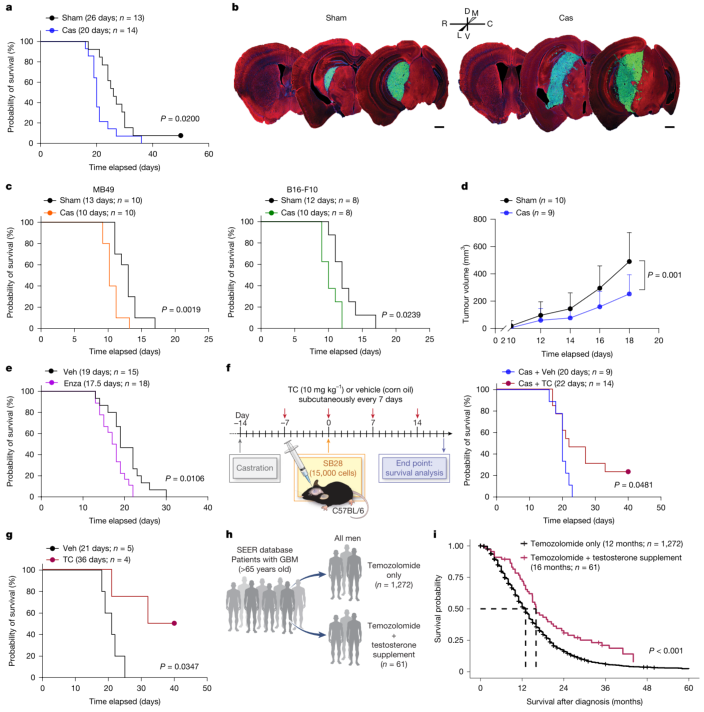
图1 | 睾酮缺失以雄激素依赖的方式导致脑肿瘤小鼠生存期缩短。 a-f,雄性小鼠在5-6周龄时进行去势或假手术,至少在肿瘤植入前2周进行。图中标示了中位生存时间和小鼠数量。数据来自两次(c、d、f)或三次(a、e)独立实验的组合。a,颅内植入SB28肿瘤后B6小鼠的生存分析。b,肿瘤植入后14天小鼠脑组织的组织学图像。微管蛋白(红色)、eGFP(SB28,绿色)、细胞核(Hoechst,蓝色)。比例尺,1 mm。解剖方位指示背侧、腹侧、吻侧、尾侧、内侧和外侧方向。c,颅内植入MB49或B16-F10肿瘤后B6小鼠的生存分析。d,B6小鼠侧腹皮下接种SB28肿瘤后的肿瘤生长曲线。e,SB28肿瘤颅内植入后,经恩杂鲁胺或溶剂处理的B6雄性小鼠的生存分析。f,g,颅内植入SB28肿瘤的去势(f)或性腺完整(g)B6雄性小鼠的生存分析,如图所示给予睾酮环丙酸酯或溶剂处理。f中的示意图展示了实验时间安排。h,i,来自SEER-Medicare数据库(2008-2019)的胶质母细胞瘤患者生存数据分析。h,数据分析示意图。i,按治疗分组调整后的Kaplan-Meier曲线。图中标示了每组的中位生存时间和患者数量。数据为均值±标准差(d)。统计方法:对数秩检验(a、c-g),双因素方差分析(d)或多变量Cox比例风险模型(i)。f和h中的插图经克利夫兰诊所基金会许可重制,©2026。
为了探究去势加速脑肿瘤生长的机制,研究团队首先排除了雄激素对肿瘤细胞的直接促增殖作用。免疫荧光分析显示,去势并未影响肿瘤细胞增殖(扩展数据图3a),反而导致肿瘤内凋亡细胞死亡标志物——切割型caspase-3水平显著下降(图2a)。这一结果提示,去势可能通过抑制抗肿瘤免疫来促进肿瘤生长。果然,在缺乏成熟T细胞和B细胞的Rag1⁻/⁻小鼠中,去势对生存期的影响完全消失(图2b)。进一步的流式细胞术分析发现,去势小鼠肿瘤浸润T细胞及外周淋巴器官(淋巴结和脾脏)中,产生抗肿瘤细胞因子IFNγ和TNF的T细胞比例显著下降(图2c、d,扩展数据图4c)。值得注意的是,在皮下肿瘤模型中,去势反而增强了T细胞功能(图2e)。通过对T细胞亚群的分析,研究人员发现,去势后脑肿瘤中终末耗竭T细胞比例增加,而效应T细胞减少;皮下肿瘤中则呈现相反模式(图2f、g),这充分表明脑肿瘤微环境中存在独特的免疫调节机制。
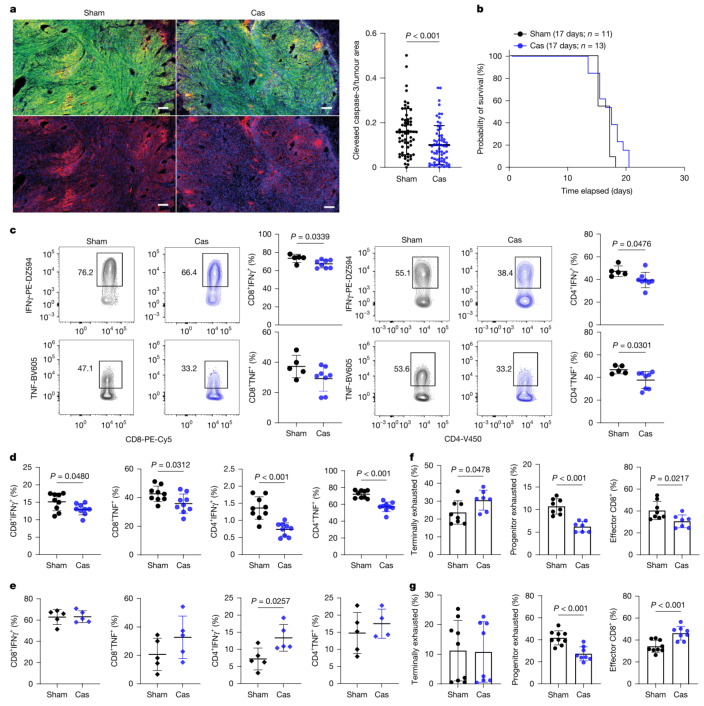
图2 | 去势诱导系统性T细胞功能衰减。 a,颅内植入SB28肿瘤后第14天,去势小鼠和假手术小鼠肿瘤组织的免疫荧光分析(每组n=5)。左图,假手术和去势荷瘤小鼠的代表性图像。切割型caspase-3(红色)、肿瘤(eGFP⁺,绿色)、细胞核(Hoechst,蓝色)。比例尺,100 μm。右图,以eGFP⁺肿瘤面积归一化的切割型caspase-3定量。P=0.000565。b,颅内植入SB28肿瘤后Rag1⁻/⁻小鼠的生存分析。数据来自四次独立实验的组合。图中标示了中位生存时间和小鼠数量。c,d,左图,脑肿瘤(SB28)植入后14天,从假手术和去势小鼠获得的T细胞的流式细胞术分析。右图,与刺激混合液孵育4小时后,测定肿瘤浸润T细胞(c)(假手术n=5,去势n=8)或腹股沟淋巴结(d)(每组n=9)中的细胞因子产生情况。P=0.000154(CD4⁺IFNγ⁺),P=0.000013(CD4⁺TNF⁺)。e,第19天测定侧腹肿瘤(SB28)浸润T细胞中的细胞因子产生情况(每组n=5)。f,g,来自脑肿瘤(f)(假手术n=8,去势n=7)或侧腹肿瘤(g)(假手术n=9,去势n=8)的CD8⁺ T细胞亚群频率。使用以下标志物鉴定T细胞亚群:终末耗竭,CD8⁺CD44⁺PD1⁺TIM3⁺TCF1⁻;祖细胞耗竭,CD8⁺CD44⁺PD1⁺TIM3⁻TCF1⁺;效应T细胞,CD8⁺CD44⁺TIM3⁻TCF1⁻。数据来自两次独立实验的组合。P=0.000053(f,祖细胞耗竭),P=0.000301(g,祖细胞耗竭),P=0.000742(g,效应T细胞)。数据为均值±标准差(a,c-g);n表示生物学独立动物数量。统计方法:非配对双尾t检验(a,c-g)或对数秩检验(b)。
进一步探索发现,去势小鼠血清中糖皮质激素(活性形式 corticosterone 及其非活性形式 11-脱氢皮质酮)水平显著升高(图3a)。使用糖皮质激素受体拮抗剂米非司酮治疗,可显著延长去势小鼠的生存期(图3b)。与此同时,去势脑肿瘤小鼠血清中促肾上腺皮质激素水平也显著升高,且这种升高在肿瘤植入后1天即出现(图3d,扩展数据图5i)。重要的是,这种效应同样具有部位特异性——颅内植入非胶质母细胞瘤细胞同样诱导ACTH升高,而皮下肿瘤则无此现象(图3e)。下丘脑神经细胞活性(c-FOS阳性细胞)在去势小鼠中显著增加(图3h),提示下丘脑-垂体-肾上腺轴处于过度激活状态。
为了阐明糖皮质激素介导免疫抑制的具体靶细胞,研究团队利用条件性基因敲除小鼠进行了一系列实验。结果显示,在T细胞特异性或调节性T细胞特异性敲除糖皮质激素受体的小鼠中,去势导致的生存期缩短和ACTH升高效应依然存在(扩展数据图7c-f)。然而,在髓系细胞特异性敲除糖皮质激素受体的LysMᶜʳᵉNr3c1ᶠˡ/ᶠˡ小鼠中,去势对生存期的影响被完全消除(图3i),尽管ACTH仍然升高(图3j)。这表明,糖皮质激素主要通过作用于髓系细胞(如巨噬细胞)来发挥免疫抑制功能。单细胞RNA测序和细胞互作分析进一步揭示,去势重塑了肿瘤微环境中的免疫细胞通讯网络,增强了免疫抑制性信号通路(如CD200、CD96、MIF等),并增加了髓系细胞与CD8⁺ T细胞之间抑制性受体-配体相互作用的概率。
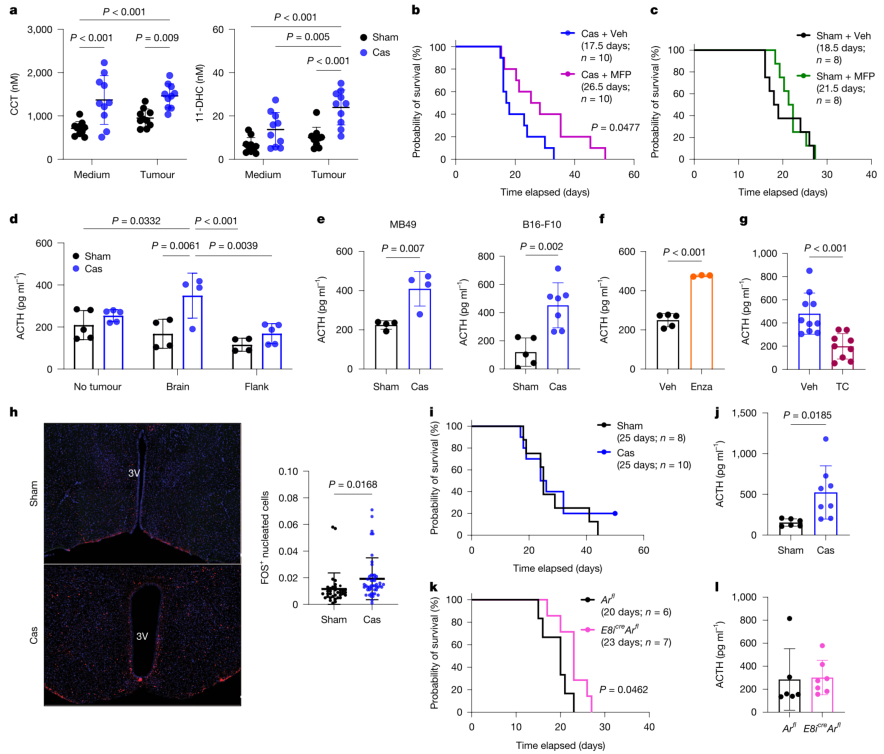
图3 | 去势脑肿瘤小鼠中下丘脑-垂体-肾上腺轴的活性增加。 a,颅内注射肿瘤(SB28)或培养基后14天收集小鼠血清,通过质谱法测定CCT和11-DHC水平。每组n=10。P=0.000661(CCT;培养基+假手术 vs 去势),P=0.000102(CCT;培养基+假手术 vs 肿瘤+去势),P=0.000003(11-DHC;培养基+假手术 vs 肿瘤+去势),P=0.000127(11-DHC;肿瘤+假手术 vs 去势)。b,c,携带SB28(脑)肿瘤的去势小鼠(b)和假手术小鼠(c)经米非司酮或溶剂治疗后的生存分析。图中标示了中位生存时间和小鼠数量。数据来自两次独立实验的组合。去势(b)和假手术(c)小鼠的实验分别进行。d,使用ELISA测定血清ACTH水平。在SB28肿瘤植入后14天(脑)或20天(侧腹)收集血清,或从无瘤小鼠收集血清。无瘤+假手术、无瘤+去势、侧腹肿瘤+去势每组n=5;脑肿瘤+假手术、脑肿瘤+去势、侧腹肿瘤+假手术每组n=4。P=0.000415(脑肿瘤+去势 vs 侧腹肿瘤+假手术)。e,颅内植入MB49(每组n=4)或B16-F10(假手术n=5,去势n=7)肿瘤后在终点测量血清ACTH水平。f,携带SB28(脑)肿瘤的性腺完整小鼠经溶剂或恩杂鲁胺治疗后的血清ACTH水平。在终点收集血清样本。溶剂组n=5,恩杂鲁胺组n=3。P=0.000003。g,携带SB28(脑)肿瘤的去势小鼠经溶剂(玉米油)或TC治疗后在终点的血清ACTH水平。实验中每组n=10,TC组n=9。数据来自两次独立实验的组合。P=0.000760。h,脑肿瘤(SB28,第14天)小鼠下丘脑中的神经活性。左图,代表性图像。FOS(红色),细胞核(Hoechst,蓝色)。比例尺,100 μm。3V,第三脑室。右图,下丘脑中FOS⁺有核细胞的定量。假手术n=5,去势n=7。i,LysMᶜʳᵉNr3c1ᶠˡ/ᶠˡ小鼠颅内植入SB28肿瘤后经假手术或去势手术的生存分析。数据来自两次独立实验的组合。图中标示了中位生存时间和小鼠数量。j,携带脑肿瘤(SB28)的LysMᶜʳᵉNr3c1ᶠˡ/ᶠˡ小鼠在第16天处死时的血清ACTH水平。假手术n=6,去势n=8。k,E8ⁱᶜᵉArᶠˡ/ᶠˡ小鼠颅内植入SB28肿瘤后的生存分析。数据来自两次独立实验的组合。图中标示了中位生存时间和小鼠数量。l,来自k图的E8ⁱᶜᵉArᶠˡ/ᶠˡ小鼠在终点测量的血清ACTH水平。Arᶠˡ/ᶠˡ组n=6,E8ⁱᶜᵉArᶠˡ/ᶠˡ组n=7。数据为均值±标准差;n表示生物学独立动物数量。统计方法:双因素方差分析加Tukey多重比较检验(a,d),对数秩检验(b,c,i,k),或非配对双尾t检验(e-h,j,l)。
那么,雄激素缺失是如何激活下丘脑-垂体-肾上腺轴的呢?研究团队对下丘脑组织进行了转录组和磷酸化蛋白组分析。结果显示,去势脑肿瘤小鼠下丘脑中与细胞因子应答相关的基因显著富集(图4a-c),且TNF和IL-1β信号通路的磷酸化水平升高(图4d)。进一步验证发现,去势小鼠脑肿瘤组织中Il1b和Tnfa mRNA表达水平显著增加(图4e)。在IL-1受体1敲除或TNF受体1/2双敲除的小鼠中,去势对生存期的影响完全消失(图4f、g)。使用抗IL-1β抗体治疗可降低去势小鼠的ACTH水平(图4h)。这些数据表明,去势后脑肿瘤诱导的神经炎症信号(IL-1β和TNF)是驱动下丘脑-垂体-肾上腺轴过度激活的关键因素。此外,在免疫缺陷NSG小鼠和人源胶质母细胞瘤异种移植模型中,同样观察到去势后ACTH升高和炎症因子表达增加,而清除小胶质细胞则可显著降低Il1b和Tnfa的表达(图4k),提示小胶质细胞在这一神经炎症反应中发挥核心作用。
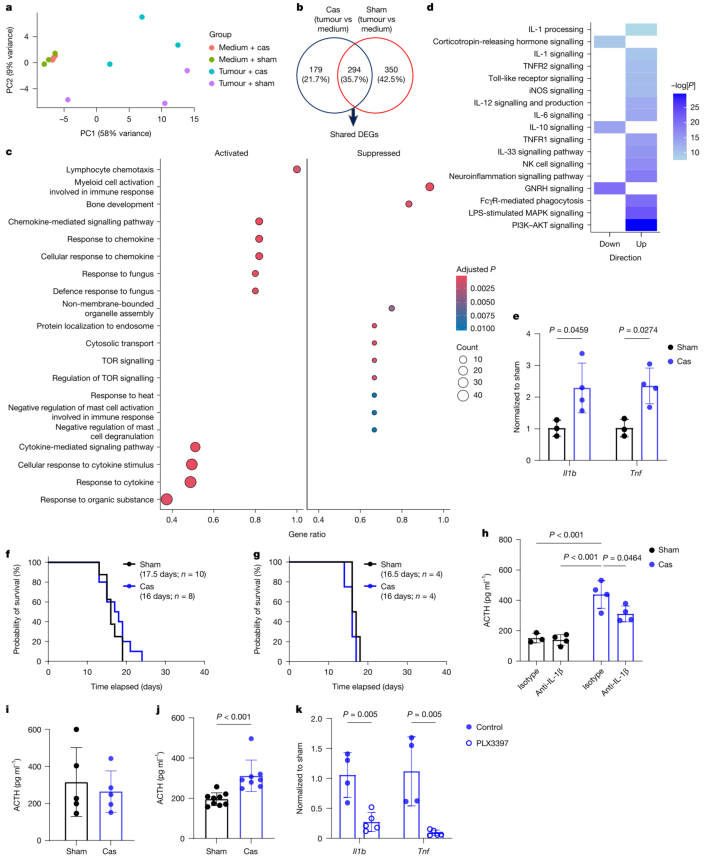
图4 | 去势通过增加脑肿瘤中的促炎细胞因子信号增强下丘脑-垂体-肾上腺轴激活。 a-c,对颅内注射SB28肿瘤细胞或培养基后第14天的去势和假手术小鼠的下丘脑样本进行RNA-seq分析(每组n=3)。a,PCA图。b,去势组和假手术组之间共享的差异表达基因。c,来自b图的共享DEGs的GO术语富集分析。d,颅内注射SB28肿瘤后第14天,去势和假手术小鼠下丘脑样本的磷酸化阵列分析。热图显示了基于磷酸化蛋白的经典通路分析,比较去势组与假手术组。e,颅内注射后第7天,假手术和去势小鼠脑肿瘤(SB28)组织中的mRNA表达水平(假手术n=3,去势n=4)。f,g,Il1r1⁻/⁻(f)和Tnfr1/2⁻/⁻(g)小鼠颅内植入SB28肿瘤后经假手术或去势手术的生存分析。图中标示了中位生存时间和小鼠数量。数据来自三次独立实验的组合。h,携带脑肿瘤(SB28)的假手术或去势小鼠经抗IL-1β抗体或同型对照抗体处理后的血清ACTH水平。数据在肿瘤植入后第7天获取,来自两次独立实验的组合。每组n=5。P=0.000500。i,Tnfr1/2⁻/⁻小鼠植入SB28肿瘤后经抗IL-1β抗体或同型对照抗体处理,在第7天测量的血清ACTH水平。每组n=5。j,颅内注射SB28细胞裂解物后第3天,假手术和去势小鼠的血清ACTH水平。数据来自两次独立实验的组合(假手术n=6,去势n=12)。P=0.006362。k,SB28肿瘤植入后第7天,饲喂PLX3397或对照饲料的去势小鼠脑组织中的Il1b和Tnfa mRNA表达水平(每组n=5)。P=0.000035(Il1b)。数据为均值±标准差;n表示生物学独立动物数量(e-k)。统计方法:双因素方差分析加Tukey多重比较检验(e),对数秩检验(f,g),非配对双尾t检验(h-k)。
为了深入解析小胶质细胞介导神经炎症的分子机制,研究团队进行了空间转录组学分析。结果显示,在肿瘤植入后第3天,去势小鼠IBA1⁺髓系细胞中NOD样受体信号通路显著激活(图5d、e),并伴随Nlrp3和Il1b表达升高(图5f)。NLRP3炎症小体是固有免疫的重要组分,其活化可促进IL-1β等炎症因子的成熟和分泌。体外实验证实,二氢睾酮处理可显著降低巨噬细胞中ASC斑点形成(炎症小体活化的标志)和IL-1β分泌(图5g、h,扩展数据图10l、m)。在体内,去势小鼠脑内IBA1⁺小胶质细胞中ASC斑点形成增加,且caspase-1的活化形式p20亚基水平升高(图5i-m)。这些结果共同表明,雄激素信号通过抑制小胶质细胞炎症小体活化来限制神经炎症,而雄激素缺失则放大了肿瘤相关炎症反应。
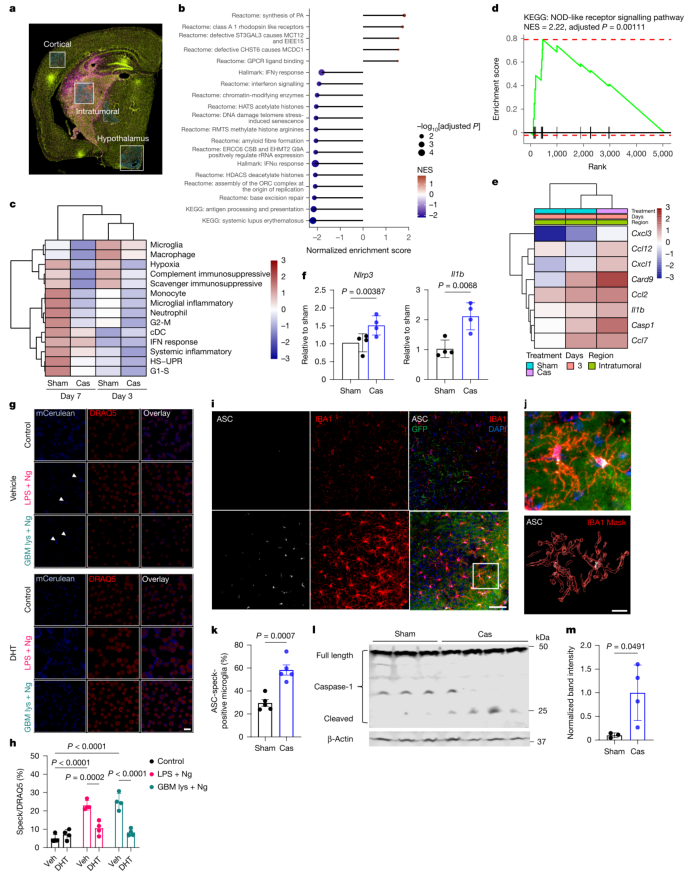
图5 | 去势脑肿瘤小鼠中增强的神经炎症由增加的小胶质细胞炎症小体活性介导。 a-e,对肿瘤(SB28)植入后第3天或第7天的假手术和去势小鼠脑组织样本进行基于Nanostring数字空间分析的空间转录组学分析(每组n=3)。a,ROI的代表性图像。b,跨所有ROI和时间点,IBA1⁺细胞在去势组与假手术组比较中的通路富集分析。c,肿瘤内区域IBA1⁺细胞中的髓系细胞特征。d,第3天肿瘤内区域IBA1⁺细胞的GSEA通路分析。e,d中排名前列基因的热图。f,颅内肿瘤(SB28)注射后第3天,假手术和去势小鼠肿瘤组织样本中的mRNA表达水平(每组n=4)。g,h,过表达ASC-mCerulean的永生化巨噬细胞的体外ASC斑点形成。经DHT(10 nM)或溶剂(甲醇)处理72小时后,细胞用LPS和尼日利亚霉素、GBM(SB28)裂解物和尼日利亚霉素刺激,或不刺激(对照)。每组n=4。g,显示ASC斑点(mCerulean;蓝色)和细胞核(DRAQ5;红色)的代表性图像。箭头指示ASC斑点。比例尺,20 μm。h,斑点阳性细胞的定量。i-k,肿瘤植入后第3天,假手术和去势脑肿瘤(SB28)小鼠脑组织中IBA1⁺小胶质细胞的体内ASC斑点形成。每组n=5。i,假手术和去势荷瘤小鼠的代表性图像。ASC(白色),IBA1(红色),SB28肿瘤(GFP;绿色),细胞核(DAPI;蓝色)。比例尺,50 μm。j,i中方框区域的放大图像和3D重建,显示IBA1⁺小胶质细胞内部的ASC斑点。比例尺,10 μm。k,斑点阳性细胞的定量。l,m,小鼠脑组织裂解物中caspase-1的免疫印迹分析。l,代表性印迹。m,切割型caspase-1(p20亚基)的定量。假手术n=3,去势n=4。数据为均值±标准差。统计方法:置换检验(b,d),非配对双尾t检验(f,k,m),或双因素方差分析加Tukey多重比较检验(g)。
综上所述,这项研究首次揭示了雄激素在脑肿瘤中的免疫保护作用,阐明了“雄激素-下丘脑-垂体-肾上腺轴-髓系细胞- T细胞”这一脑特异性免疫调节轴。研究指出,胶质母细胞瘤的诊断中位年龄为68-70岁,恰好与男性睾酮水平随年龄下降的时期重合。真实世界数据分析提示,对于65岁以上男性患者,睾酮补充与显著延长的生存期相关。尽管小鼠模型无法完全模拟人类胶质母细胞瘤的复杂性,但这些发现为理解睾酮、神经炎症和免疫调节在脑肿瘤中的交叉作用提供了重要框架。未来研究需关注衰老背景下雄激素对脑肿瘤的影响,并谨慎考虑临床中地塞米松(用于控制脑水肿)与睾酮下降的联合效应。这项工作不仅凸显了中枢神经系统免疫应答的独特性,更强调了将性别作为生物学变量纳入脑肿瘤研究的重要性,有望为脑肿瘤的个性化免疫治疗开辟新方向。


