【神麻人智】迈向术后认知功能障碍的精准风险分层:骨科手术中术前炎症与神经退行性蛋白生物标志物的系统综述
时间:2026-05-09 21:36:39 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
图文摘要
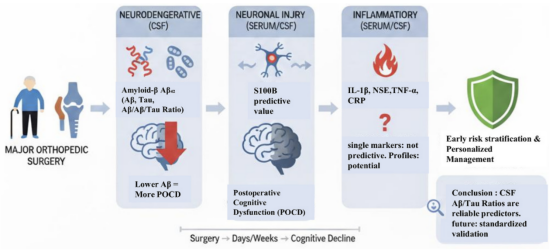
亮点
• 脑脊液Aβ/tau生物标志物可预测骨科手术后的术后认知功能障碍。
• 单一血清生物标志物在术前POCD风险预测中显示出有限且不一致的价值。
• 多标志物炎症组合在预测认知下降方面优于单一蛋白。
• 需要标准化的生物标志物和POCD定义以进行术前临床风险分层。
背景:
术后认知功能障碍(Postoperative Cognitive Dysfunction,POCD)是老年患者接受大型手术后常见的并发症,与术后恢复延迟及长期认知功能下降密切相关。识别可靠的术前蛋白质生物标志物有助于实现早期风险分层,并促进个体化围手术期管理。
方法:
本研究对评估术前炎症及神经退行性蛋白生物标志物与术后POCD关系的前瞻性队列研究进行了系统综述。检索数据库包括 PubMed、Embase、Web of Science、Cochrane CENTRAL 和 Scopus,时间范围为建库至2025年10月30日。纳入研究需在术前检测血液或脑脊液(CSF)中的蛋白生物标志物,并报告标准化的术后认知结局。采用 Newcastle–Ottawa 量表评估研究的偏倚风险。由于生物标志物类型、检测方法及POCD定义存在异质性,本研究采用叙述性综合方法进行结果整合。
结果:
共纳入6项前瞻性队列研究,涉及705例接受大型骨科手术的患者。所评估的生物标志物包括炎症细胞因子(IL-1β、IL-6、TNF-α、IL-8、CRP)、神经元及胶质细胞损伤标志物(S100B、NSE、GFAP、NFL),以及与阿尔茨海默病相关的脑脊液蛋白(Aβ1-42、Aβ40、总tau及磷酸化tau)。研究发现,术前脑脊液中Aβ1-42水平降低及Aβ/tau比值下降是预测POCD最为一致的指标。相比之下,单一血清生物标志物(包括S100B及炎症细胞因子)的预测价值表现不稳定或较为有限。而复合炎症标志物谱在识别长期认知功能下降高风险患者方面显示出一定潜力。
结论:
现有研究表明,术前脑脊液中淀粉样蛋白相关生物标志物与POCD之间的关联相对更为显著;然而总体证据仍然有限,尚需进一步验证。同时,多标志物炎症特征可能有助于提高风险评估能力。未来仍需开展标准化研究,以支持其在临床中的应用。
1.引言:
术后认知功能障碍(Postoperative Cognitive Dysfunction,POCD)是围手术期医学中的一项重要挑战,尤其在老年人群中更为突出,其在大型非心脏手术后的发生率可高达41.4%。该综合征表现为术后认知功能下降,包括记忆、注意力及执行功能受损,对患者的生活质量及术后恢复产生显著不利影响。POCD不仅带来短期问题,如住院时间延长及医疗费用增加,还与长期不良结局相关,包括认知功能加速衰退及死亡风险增加。
POCD的发病机制具有多因素特征,涉及神经炎症反应、神经元损伤以及麻醉药物的影响。其中,神经炎症被认为是关键致病因素之一。已有研究表明,手术可诱导炎症反应,从而破坏血脑屏障(blood-brain barrier,BBB)。此外,基质金属蛋白酶-9(MMP-9)及S100B等生物标志物已被证实与术后认知功能受损相关。在麻醉策略方面,一些特定方法(如使用右美托咪定)通过模拟自然睡眠状态并减轻神经炎症反应,可能降低POCD的发生率。
当前POCD研究中的一个关键不足在于缺乏能够预测术后认知功能障碍发生及严重程度的可靠术前生物标志物。新兴证据提示,某些生物学指标可能作为POCD风险预测因子,帮助临床医生根据患者对认知功能下降的易感性进行风险分层。研究者强调,应进一步开发并验证此类标志物,以促进靶向干预及个体化麻醉策略的实施。目前,POCD主要通过神经心理学测试进行诊断,但不同研究所采用的测试工具存在差异,且易受文化、语言及教育水平等因素影响,从而限制其在临床中的可靠性。
在此背景下,分子生物标志物为实现客观风险预测提供了有前景的途径。既往研究主要集中于术后神经损伤相关标志物,如S100B、神经元特异性烯醇化酶(NSE)、淀粉样蛋白β(Aβ)、tau蛋白、神经丝轻链(NFL)及胶质纤维酸性蛋白(GFAP),这些指标可反映手术及麻醉对大脑的应激程度。然而,这些标志物通常在神经损伤发生后才升高,限制了其在早期预防中的应用价值。相比之下,术前蛋白生物标志物有望在手术前识别高风险人群。神经退行性或炎症相关蛋白(如Aβ、tau、NSE、S100B等)的基础水平变化,已被认为与神经系统抵抗力下降及围手术期损伤易感性增加相关。明确其预测价值,有助于实现患者风险分层、指导围手术期管理并制定预防策略。
在认知功能正常的老年人群中,多种神经退行性及炎症相关蛋白在基线状态下即可检测到,且其水平可能随年龄增长、血管共病或亚临床神经退行性改变而发生变化。例如,在无明显神经系统疾病的老年个体中,循环中的S100B及细胞因子通常处于可检测的生理范围内,而脑脊液中Aβ1-42水平则随年龄逐渐下降 。值得注意的是,在随后发生POCD的患者中,其术前生物标志物水平往往仍处于上述正常生理范围内,这使得难以判断观察到的差异究竟代表病理性异常,还是正常生理波动范围内的相对变化。明确这一点对于正确解读术前生物标志物的临床意义及预测价值至关重要。
尽管如此,目前相关证据仍较为零散,关于术前生物标志物在POCD诊断中的准确性尚未形成一致结论。此外,需要注意的是,围手术期认知研究的术语体系已发生演变。根据2018年国际共识建议,围手术期神经认知障碍(perioperative neurocognitive disorders,PND)包括术后谵妄(即术后早期出现的注意力波动性障碍)、延迟性神经认知恢复(30天内认知下降)以及术后神经认知障碍(持续至12个月的认知损害)。然而,许多纳入研究发表于该命名更新之前,仍使用“POCD”这一术语。因此,在本综述中,我们保留原研究所使用的术语,并在有报告时区分POCD与术后谵妄,同时在解释结果时考虑这些定义差异。
基于上述背景,本研究开展系统综述,以综合当前关于术前蛋白生物标志物与术后认知功能障碍之间关系的证据。研究旨在明确哪些生物标志物具有潜在预测价值,并探讨标志物类型、样本来源及手术特征对该关联的影响。
2.方法(Methods)
本系统综述按照系统评价与Meta分析优先报告项目(Preferred Reporting Items for Systematic Reviews and Meta-Analyses,PRISMA)声明进行报告。研究方案已在 PROSPERO 注册库进行前瞻性注册(注册号:CRD420251230960)。
2.1 数据来源与检索策略
我们对人群研究进行了系统检索,纳入对象为在术前检测血液或脑脊液(cerebrospinal fluid,CSF)中蛋白质生物标志物,并报告术后认知功能障碍结局的研究。检索数据库包括 PubMed、Embase、Web of Science、Cochrane CENTRAL 以及 Scopus,检索时间范围为各数据库建库至2025年10月30日的所有记录。
此外,我们还通过查阅已纳入文献及相关综述的参考文献列表,补充检索潜在相关研究。检索策略综合使用以下关键词:
认知结局相关术语:如“术后认知功能障碍”(postoperative cognitive dysfunction)、“术后谵妄”(postoperative delirium)、“术后神经认知障碍”(postoperative neurocognitive disorder);
蛋白生物标志物相关术语:如 S100B、淀粉样蛋白β1–42(Aβ1–42)、tau 蛋白、白细胞介素-6(IL-6)、C反应蛋白(CRP)、biomarker、protein;
围手术期时间相关术语:如术前(preoperative)、基线(baseline)、术前阶段(pre-op)。
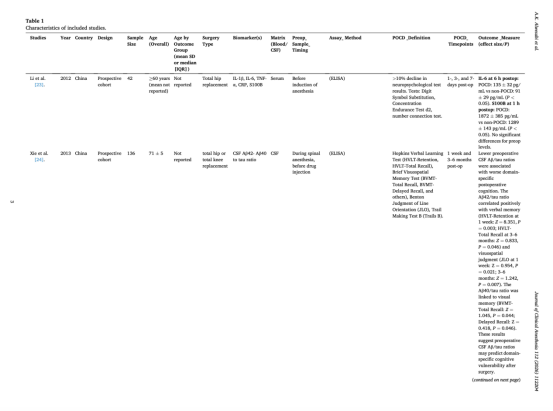
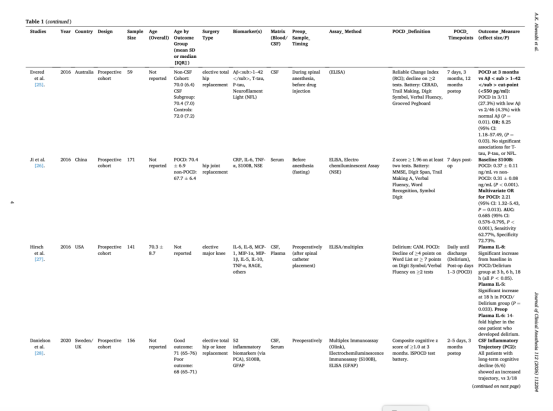
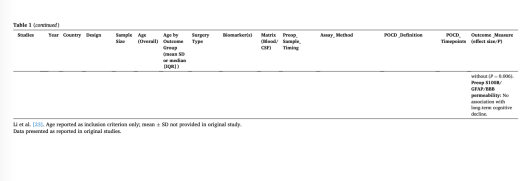
各数据库的完整检索式详见补充材料(表1)。
2.2 纳入与排除标准(Eligibility criteria)
纳入符合以下条件的研究:
1. 研究对象为接受骨科手术的人类受试者;
2. 在术前检测血液(血清或血浆)或脑脊液中的蛋白质生物标志物;
3. 报告术后认知结局,包括POCD、术后谵妄(postoperative delirium,POD)或其他结构化神经认知评估结果。
排除标准如下:
1. 动物实验或基础研究;
2. 综述、系统综述或Meta分析;
3. 病例报告;
4. 无全文的会议摘要;
5. 未明确界定POCD评估方法或缺乏适当对照组的研究。
2.3 文献筛选(Study selection)
完成文献检索后,将所有检索结果导入 EndNote X9(Clarivate Analytics)进行系统管理。由两名独立研究者(JYX 和 JXX)进行文献筛选。筛选过程中,研究者根据预设的纳入与排除标准对标题和摘要进行评估,并记录所有被排除文献的具体原因。
通过初筛的文献进入全文评估阶段。如两位研究者之间存在分歧,则通过与第三位研究者(YTL)讨论达成一致。
2.4 数据提取(Data extraction)
由两名研究者(BXG 和 YHM)独立使用预先设计的数据提取表进行数据提取。提取内容包括:
研究基本信息:作者、发表年份、研究国家;
研究设计及样本量;
受试者基本特征:年龄、性别;
手术类型;
所测量的生物标志物;
样本类型:血清、血浆或脑脊液;
检测方法;
术前样本采集时间;
POCD的定义及评估工具;
POCD评估时间点;
统计指标:包括各结局组生物标志物水平的均值/标准差、比值比(OR)、风险比(HR)、曲线下面积(AUC)、95%置信区间(CI)及P值。
对于缺失或不明确的数据,必要时联系原研究的通讯作者以获取补充信息。
2.5 质量评价(Quality assessment)
纳入研究的方法学质量由两名研究者(AKA 和 BXG)独立采用 Newcastle–Ottawa 量表(Newcastle–Ottawa Scale,NOS)进行评估。该量表被推荐用于评价观察性队列研究(包括前瞻性研究)的偏倚风险。NOS从三个方面对研究质量进行评估:
研究对象选择(最高4分)
队列可比性(最高2分)
结局评估及随访充分性(最高3分)
根据总评分,将研究质量划分为:
高质量(7–9分)
中等质量(4–6分)
低质量(<4分)
两位研究者之间的任何分歧均通过与第三位研究者(YTL)讨论解决。
2.6 结局指标(Outcome measures)
鉴于围手术期认知研究领域的术语不断演变,本研究对纳入文献中标记为POCD的结局,均按照原研究作者所采用的定义进行整合分析。对于报告了术后谵妄(postoperative delirium,POD)的研究,则单独进行分析。由于大多数纳入研究发表于围手术期神经认知障碍(perioperative neurocognitive disorders,PND)命名体系正式提出之前,本研究未对其结局进行重新归类。
本研究的主要结局为术后认知功能障碍(POCD),其定义依据各纳入研究原始标准。POCD通常通过经验证的神经心理学测试量表进行评估,包括:
国际POCD研究(ISPOCD)测试组合
Hopkins言语学习测验(Hopkins Verbal Learning Test)
简式视觉空间记忆测验(Brief Visuospatial Memory Test)
连线测验(Trail Making Tests)
数字符号替代测验(Digit Symbol Substitution)
言语流畅性测试(Verbal Fluency)
综合认知Z评分
各研究中POCD的定义存在差异,常见判定标准包括:
可靠变化指数(Reliable Change Index)
Z评分阈值(如≥2项测试中Z值下降≥1.96)
预设的临界值(cut-off)
次要结局包括术后谵妄(POD)(如有报告),通常采用标准化工具进行评估,例如意识模糊评估法(Confusion Assessment Method,CAM)。此外,还包括基于单项认知测试评分评估的特定认知领域功能变化,如:言语记忆、视觉空间能力、执行功能
纳入研究还报告了其他结局指标,包括生物标志物动态变化(术前与术后水平变化)及其与早期或长期术后认知下降之间的关联。若有报告,不良事件也被提取,但在纳入的前瞻性队列研究中相关数据较少。
鉴于各研究在术后认知评估时间点方面存在较大差异,本研究按照原始报告时间点对结局进行描述性整合,而未将其统一视为相同临床实体进行合并分析。
2.7 数据综合方法(Data synthesis approach)
由于纳入研究均为前瞻性队列设计,且在生物标志物类型、检测方法、生物标志物采集时间以及POCD定义等方面存在显著异质性,本研究采用叙述性综合方法对数据进行整合。
根据生物学机制对研究进行分组,包括:
阿尔茨海默病相关标志物(Aβ、tau)
神经损伤标志物(S100B、NSE)
炎症标志物(如IL-6、IL-1β、TNF-α、CRP)
多标志物炎症组合
针对每一类生物标志物,我们总结其与POCD之间关联的方向、统计学显著性以及(在可获得时)效应量指标。
尽管按照生物学机制对标志物进行分类有助于结构化分析,但需要认识到,POCD的发生不仅受分子层面因素影响,还受到多种围手术期因素的共同作用,包括麻醉方式、术中血流动力学状态、全身炎症反应、基线认知储备以及脑血管完整性等。因此,在结果综合过程中,生物标志物与POCD之间的关联均结合更广泛的临床及围手术期背景进行解释。
由于纳入研究在认知评估工具、POCD定义、生物标志物检测基质(血清、血浆或脑脊液)以及术后评估时间点等方面差异较大,因此不适合采用Meta分析对效应量进行合并。
相反,本研究采用定性比较方法,重点识别一致性模式(例如:术前S100B升高与POCD风险增加相关;脑脊液Aβ/tau比值降低可预测特定认知领域的下降),同时分析不同研究之间的差异。
此外,我们还考虑了方法学差异对结果的影响,包括检测平台(如ELISA、多重免疫分析)、生物标志物测量时间(基线水平与术后动态变化)以及手术类型(如髋关节与膝关节置换)。除方法学差异外,各研究之间还存在显著的临床异质性,包括生物标志物采样时间、术后认知评估的时间与持续时间、麻醉技术、围手术期管理策略以及协变量调整方法的不同。这些差异直接影响POCD及术后谵妄(POD)的发生率及检测,从而限制了跨研究比较的可比性,并阻碍了有意义的定量整合。在分析相关性时已充分考虑上述因素。
2.8 证据质量评估(Certainty of evidence)
采用GRADE方法对关键生物标志物与POCD之间关联的证据总体质量进行评估。由于所有纳入研究均为前瞻性观察性队列研究,其初始证据等级设定为低等级。在此基础上,根据偏倚风险、不一致性、间接性及不精确性等因素对证据质量进行进一步降级(如适用)。
3. 结果(Results)
3.1 文献筛选(Study selection)
通过五个数据库共检索获得512条文献记录。去除235条重复文献后,剩余277条文献进入筛选阶段。经标题及摘要筛选,共排除252条文献。随后对25篇文献进行全文评估,其中19篇被排除。最终,共有6项研究纳入本系统综述 。详细筛选流程见图1。
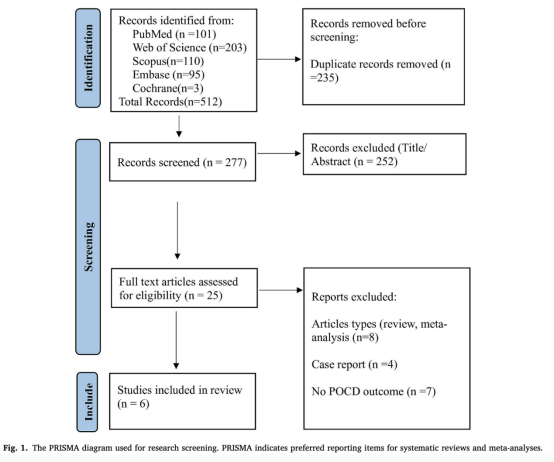
3.2 纳入研究特征(Characteristics of included studies)
本研究共纳入6项前瞻性队列研究,涉及705名受试者。其中,仅有2项研究报告了亚组数据(如POCD组与非POCD组);这些亚组数据属于各研究内部的分层分析,不影响总体样本量。
纳入研究分别来自中国、澳大利亚、美国、瑞典及英国。研究对象主要为接受大型骨科手术的老年患者,包括全髋关节或全膝关节置换术。
在这6项研究中,评估的围手术期生物标志物类型较为广泛,主要包括:
炎症细胞因子:IL-1β、IL-6、TNF-α、IL-8、C反应蛋白(CRP)
神经元及胶质细胞损伤标志物:S100B、神经元特异性烯醇化酶(NSE)、胶质纤维酸性蛋白(GFAP)、神经丝轻链(NFL)
阿尔茨海默病相关脑脊液蛋白:Aβ1-42、Aβ40、总tau及磷酸化tau
生物标志物样本来源包括血清或脑脊液,通常在麻醉诱导前或蛛网膜下腔导管置入后立即采集。检测方法主要包括酶联免疫吸附测定(ELISA)、多重免疫分析以及电化学发光免疫分析。
各研究中POCD的定义存在差异,但通常采用标准化神经心理学评估方法,包括:
基于Z评分的判定标准
可靠变化指数(Reliable Change Index)
国际POCD研究(ISPOCD)测试组合
术后认知随访时间从早期(术后1–7天)到长期(术后3–12个月)不等。
3.3 研究偏倚风险(Risk of bias in the studies)
本综述采用 Newcastle–Ottawa 量表(NOS)对纳入的6项前瞻性队列研究的方法学质量及潜在偏倚进行评估,评估结果见图2A和图2B。
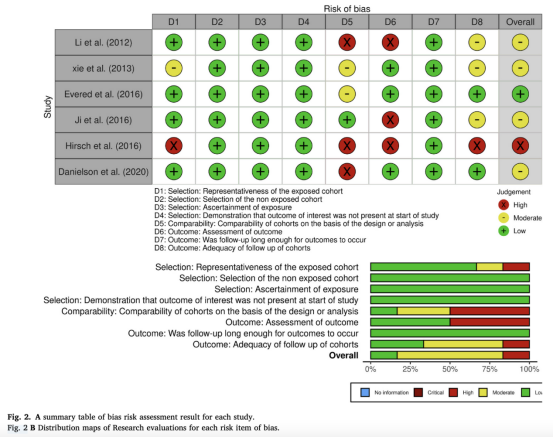
在6项研究中:
4项被评定为整体偏倚风险较低,提示其研究方法较为严谨,结果具有较高可靠性;
其余2项研究由于方法学细节报告不足,在可靠性评估方面存在一定不确定性。
从具体评价维度来看:
研究对象选择方面:整体表现较好,多数研究能够满足暴露组代表性及非暴露组选择的要求;但部分研究未充分证明研究开始时结局尚未发生。
队列可比性方面:大多数研究能够满足可比性标准,并对队列选择提供合理说明,但少数研究在该方面存在一定局限。
结局评估方面:整体评价较为积极,多数研究在结局评估方法及随访完整性方面表现良好;但个别研究在随访时间长度及结局评估方法方面仍存在中等程度的不确定性。
3.4 证据质量(Certainty of evidence)
根据GRADE评价体系,术前生物标志物与POCD之间关联的证据质量总体范围为低至极低(见补充表1)。其中:
脑脊液淀粉样蛋白相关标志物的证据质量评定为低等级;
血清S100B、炎症细胞因子以及多标志物蛋白组学分析的证据质量评定为极低等级,主要原因在于研究结果之间存在不一致性及统计精确性不足。
3.5 结局(Outcomes)
3.5.1 主要结局(Primary outcome)
6项前瞻性队列研究探讨了术前蛋白质生物标志物与接受大型骨科手术的老年患者发生术后认知功能障碍(POCD)之间的关系。在这些研究中,评估的生物标志物范围广泛,包括:
炎症细胞因子:IL-1β、IL-6、TNF-α、CRP
神经元及胶质细胞损伤标志物:S100B、NSE、GFAP、神经丝轻链(NFL)
阿尔茨海默病相关蛋白:Aβ1-42、Aβ40、总tau、磷酸化tau以及Aβ/tau比值
生物标志物检测方法包括酶联免疫吸附测定(ELISA)、电化学发光免疫分析及多重蛋白组学平台。术后认知结局的评估时间范围从早期术后阶段延续至3–12个月。
在单一生物标志物中,S100B与POCD的关联最为一致。Ji等[26]研究发现,在术后第7天发生POCD的患者中,其术前S100B水平显著高于未发生POCD者(0.37 ± 0.11 vs. 0.31 ± 0.08 ng/mL,P < 0.001);多变量分析进一步证实S100B为独立预测因素(OR = 2.21,95% CI:1.32–5.43,P = 0.013,AUC = 0.685,95% CI:0.576–0.795)。然而,其他研究未能重复这一结果。例如,Li等未发现POCD组与非POCD组在术前IL-1β、IL-6、TNF-α、CRP或S100B水平方面存在显著差异,但POCD患者术后IL-6和S100B升高更为明显。类似地,Danielson等发现,包括S100B、GFAP及52种炎症蛋白在内的多种术前血清标志物均未与术后3个月的认知下降相关。
相比之下,针对阿尔茨海默病相关蛋白的研究显示出更稳定的关联性。Xie等报道,术前较低的Aβ1-42/tau及Aβ40/tau比值与术后1周及3–6个月的言语记忆及视觉空间能力下降显著相关。Evered等进一步证实,较低的Aβ1-42水平可预测术后3个月POCD的发生,而在其研究中,总tau、磷酸化tau及NFL未表现出预测价值。
Hirsch等评估了多种炎症细胞因子,未发现POCD组与非POCD组在术前水平上的显著差异,但术后IL-8及IL-5升高与POCD和/或术后谵妄(POD)相关。Danielson等则发现,尽管单一蛋白未显示预测能力,但基于高维蛋白组学分析构建的复合炎症模式(主成分PC2)能够准确识别所有发生长期认知下降的患者(P = 0.006)。
总体而言,各研究中最为一致的POCD预测指标为术前脑脊液淀粉样蛋白相关标志物,尤其是Aβ1-42水平降低及Aβ/tau比值下降;而单一血清生物标志物的预测结果则表现出较大的不一致性。相比之下,多标志物炎症特征可能较单一蛋白具有更强的预测潜力。
需要指出的是,各研究在POCD定义、生物标志物检测平台、样本类型、认知评估方法以及术后随访时间点(从术后数日至12个月不等)方面存在显著差异,从而导致较高的研究异质性。此外,早期术后认知下降与长期神经认知障碍可能代表不同的临床轨迹,因此在跨研究比较时需谨慎解读相关结果。
3.5.2 其他结局(Other outcomes)
部分纳入研究还报告了其他术后神经系统及炎症相关发现。尽管这些结果未纳入主要分析,但为理解术后认知易感性提供了重要补充背景。
Hirsch等观察到,发生POCD和/或术后谵妄(POD)的患者在术后血浆IL-8和IL-5水平升高更为显著,提示围手术期炎症反应增强可能参与早期神经功能紊乱的发生。然而,在其研究队列中,仅有1例患者被确诊为谵妄,且所有术前生物标志物均未能可靠预测其发生。
Danielson等对长期认知变化进行了分析。研究发现,尽管术前单一蛋白(如S100B、GFAP及血脑屏障通透性指标)与术后3个月认知下降无显著关联,但基于脑脊液炎症特征构建的动态变化模式(主成分PC2)与持续性认知损害显著相关。这一结果强调了复合生物标志物模式在识别长期术后认知功能恶化高风险患者中的潜在价值。
此外,Li等及Hirsch等均报告,在发生POCD的患者中,术后炎症细胞因子(包括IL-6、IL-8及IL-5)显著升高。尽管这些变化可能反映手术应激所诱导的过度神经炎症反应,但其术前水平并未能够稳定区分后续发生POCD的个体。
总体而言,现有证据表明,术前淀粉样蛋白相关标志物仍是POCD最有力的预测指标;而炎症细胞因子更多反映围手术期动态变化,而非基础风险状态。最新研究进一步提示,多标志物炎症动态轨迹可能较单一蛋白具有更高的预测价值,但仍需开展更大规模、标准化的研究,以验证相关发现并建立具有临床意义的生物标志物阈值。
4. 讨论(Discussion)
本系统综述综合了当前关于术前蛋白质生物标志物预测接受大型骨科手术老年患者术后认知功能障碍(POCD)的相关证据。基于6项前瞻性队列研究的结果,研究呈现出若干一致性结论。其中,最为可靠的预测指标为脑脊液淀粉样蛋白相关标志物,尤其是Aβ1-42水平降低及Aβ/tau比值下降。多项研究表明,这些指标与术后早期及长期认知功能下降均具有显著相关性。该结果与阿尔茨海默病相关的病理生理机制相一致,即脑脊液Aβ1-42水平降低反映脑内淀粉样蛋白沉积增加。此类潜在的神经退行性易感性可能使部分个体更易受到手术应激影响,从而发生术后认知功能下降(见图3A)。
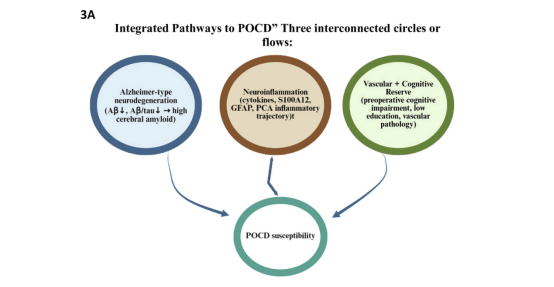
尽管脑脊液淀粉样蛋白相关标志物在预测性能方面表现较优,但其在临床常规术前风险分层中的应用仍面临较大挑战。脑脊液采集具有侵入性,且需要较高的资源投入,在大多数骨科手术患者中并非常规操作。除操作本身的侵入性外,脑脊液标志物检测还涉及较高的经济成本及复杂的实验室条件,包括检测平台建设及较长的结果获取时间。从成本效益角度来看,除非未来研究能够证实其具有较高预测准确性并能显著改善围手术期管理及临床结局,否则难以支持将术前腰穿作为常规风险评估手段。此外,仅有两项研究评估了脑脊液淀粉样蛋白标志物,这在一定程度上限制了相关结论的稳健性及外推性。
相比之下,基于血清或血浆的多标志物炎症特征虽然在单一指标层面的预测能力较弱,但由于其微创性及更易融入围手术期流程,具有更高的临床可行性。因此,未来研究应优先关注可及性更高的血液生物标志物组合,并在更大规模、多中心队列中进行验证,同时建立标准化阈值体系。
在神经损伤相关血清标志物中,尤其是S100B,其预测价值表现有限且结果不一致。Ji等发现术前S100B升高为POCD的独立预测因素。然而,该研究中POCD组与非POCD组之间S100B水平的绝对差异较小,且其数值多仍处于无明显神经系统疾病老年人群的正常范围内。这种微小差异(约0.05–0.1 ng/mL)的临床意义尚不明确,尤其是在缺乏围手术期特异性阈值的情况下。此外,其他研究未能重复这一结果。由于S100B不仅来源于中枢神经系统,还可来源于外周组织,其诊断特异性受到限制,可能无法准确反映脑损伤程度。
同样,术前炎症细胞因子(如IL-1β、IL-6、TNF-α、CRP)在不同研究中的预测价值较弱且不一致。这种差异可能与其生物学变异性较大、来源多为外周以及对采样时间和全身状态高度敏感有关。尽管如此,多项研究仍发现,在发生POCD和/或术后谵妄(POD)的患者中,术后炎症因子水平显著升高 ,这一结果支持了手术诱导神经炎症在POCD发生中的关键作用。
值得关注的是,蛋白组学炎症特征分析提供了新的研究方向。Danielson等通过主成分分析构建的脑脊液炎症动态变化模式,能够准确识别所有发生长期POCD的患者,其预测性能优于单一生物标志物。这一发现提示,POCD是一种由炎症与神经退行性过程相互作用驱动的多因素疾病,多标志物联合模式可能优于单一指标在风险预测中的表现(见图3B)。
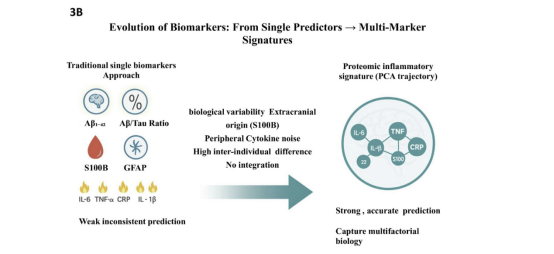
需要强调的是,基于生物标志物的易感性评估不应孤立解读。POCD的发生受多种围手术期因素调控,包括麻醉深度、手术时长、全身炎症反应程度、脑灌注稳定性以及既往血管性或认知功能损害等。这些因素可能与个体的神经退行性或炎症易感性相互作用,共同加重术后认知功能损害。因此,尽管生物标志物分类有助于揭示潜在机制,但在临床风险预测中,必须整合分子、生理及围手术期多维因素。未来研究应构建多维预测模型,将生物标志物与围手术期监测指标及基线认知评估相结合,以提高预测准确性。
现有文献亦支持围手术期炎症与认知结局之间的关联。例如,皮质醇水平升高与术后谵妄发生相关,而S100A12等蛋白亦被证实与认知功能障碍相关。此外,人口学及基线认知因素(如教育水平较低、多任务处理能力受损)同样会影响认知易感性。这些发现进一步强调了POCD的多因素本质,即炎症状态、认知储备、心理社会特征及神经退行性负荷共同决定术后认知结局。
除生物标志物外,围手术期监测策略亦可能对风险产生影响。
双频指数(bispectral index,BIS)监测通过减少麻醉深度波动,已被证实与POCD发生率降低相关;此外,脑氧监测研究提示,通过优化术中脑灌注亦可能进一步降低认知损伤风险。这些研究表明,将生物标志物与生理监测及认知评估相结合的综合围手术期管理策略,可能为高风险患者提供最为有效的保护。
针对神经炎症标志物的研究(如GFAP、S100蛋白及细胞因子谱)同样表明,炎症活动水平与术后认知功能下降之间存在相关性 。此外,术前认知功能受损已被广泛认为是不良术后结局的重要预测因素,提示有必要在术前进行系统性的认知功能评估。
麻醉方式亦可能影响术后认知结局。例如,有研究发现地氟烷与七氟烷在术后认知恢复方面存在差异。然而,本综述纳入的研究未能系统性地根据麻醉方式(全身麻醉与区域麻醉)进行分层分析,从而限制了对潜在效应修饰因素的评估。鉴于麻醉暴露可能通过调节神经炎症通路影响认知结局,未来研究应进一步探讨不同麻醉技术下生物标志物预测性能的差异。
脑血管完整性及既往血管病变同样对认知功能轨迹产生重要影响,这一点已在Vemuri等及Demakakos等的研究中得到证实。总体而言,这些证据共同强调,POCD的发生源于神经退行性改变、炎症反应、血管因素及认知基础状态之间的复杂相互作用。
本综述亦存在一定局限性。首先,仅有6项研究符合纳入标准,限制了研究结果的外推性。尽管曾考虑进行定量Meta分析,但由于研究之间存在显著的方法学及临床异质性,最终未实施统计合并分析。具体而言,各研究在生物标志物类别(淀粉样蛋白、神经损伤标志物、炎症标志物)、样本来源(脑脊液与血清)、检测方法以及标志物采样时间方面差异较大。
此外,术后认知结局的评估方法亦不统一,包括不同的神经心理测试量表、不同的POCD诊断阈值,以及不同的随访时间(从术后1–7天至3个月或12个月不等)。早期术后认知下降、延迟性神经认知恢复以及长期术后神经认知障碍在概念上相关,但在临床上属于不同实体。因此,评估时间点的差异可能导致结局分类偏倚,并影响生物标志物关联结果的解释。短期随访研究可能更多反映暂时性的炎症反应,而长期随访则更可能揭示潜在的神经退行性易感性。这种时间维度上的差异进一步限制了研究结果的统计整合能力,并削弱了不同研究之间的直接可比性。
此外,显著的临床异质性亦进一步限制了结果的解释。不同研究在生物标志物检测时间、术后认知评估间隔(从数天至数月不等)以及随访时间长度方面存在较大差异。早期术后认知功能障碍、延迟性神经认知恢复以及长期术后认知功能损害在概念上存在重叠,但属于相互独立的临床实体,不同的随访时间长度可能对研究中所观察到的关联关系产生影响。此外,各研究在围手术期混杂因素的调整方面存在显著差异。诸如麻醉暴露、术中低血压、脑灌注状态、术后并发症、基线认知储备以及血管性共病等关键因素并未得到一致控制。这些差异可能引入残余混杂,从而影响生物标志物与POCD之间关联的强度及方向。对早期术后认知下降与长期术后神经认知障碍进行分层分析,可能具有重要意义。炎症相关生物标志物更可能预测短暂的早期认知功能异常,而神经退行性相关标志物则可能与持续性认知损害更为密切相关。
另一项重要局限在于纳入研究对潜在混杂因素的调整不充分且不一致。影响术后认知结局的关键因素,如基线认知状态、教育水平(认知储备)、衰弱状态、抑郁症状、血管性共病及麻醉方式等,在多变量分析中未被系统纳入。尽管部分研究对部分人口学或临床变量进行了调整,但缺乏全面的风险建模。因此,残余混杂可能对观察到的生物标志物关联产生影响,从而限制因果推断能力及预测结果的外推性。未来研究应在多变量预测模型中整合生物标志物谱、标准化的认知储备评估、衰弱指数、血管负荷指标以及围手术期管理变量,以提高预测模型的准确性与临床适用性。
此外,各研究在POCD定义及神经心理学测试工具方面存在较大差异,增加了不同研究之间直接比较的难度。多数研究为小样本、单中心设计,这在一定程度上限制了研究结果的外部效度。
值得注意的是,所有纳入研究均针对接受大型骨科手术的患者,主要包括全髋或全膝关节置换术。然而,由于报告信息有限,未能开展不同手术类型(如髋关节与膝关节置换)之间的亚组分析。不同手术在手术时长、失血量、炎症反应程度及围手术期应激方面存在差异,这些因素均可能影响生物标志物动态变化及POCD发生风险。未来研究应进一步探讨不同手术类型对生物标志物预测性能的影响。
尽管骨科手术可作为老年患者手术应激的典型模型,但本研究结果未必可直接推广至其他高风险手术类型(如心脏、血管、腹部或神经外科手术)。在这些手术中,炎症负荷、体外循环暴露、脑栓塞风险及血流动力学波动等因素可能存在显著差异。因此,在将生物标志物的预测性能推广至其他手术人群时,应保持谨慎态度。
最后,需要指出的是,大多数研究仅在单一术前时间点对生物标志物进行测量,这限制了对动态纵向变化的观察,而此类变化可能更能反映神经炎症过程的真实演变。另一项重要局限在于,目前围手术期环境下多数生物标志物尚缺乏标准化的病理学阈值。在缺乏针对手术人群验证的界值标准的情况下,尚难明确观察到的关联究竟代表具有临床意义的异常,还是仅反映生理范围内的统计学差异。
尽管存在上述局限,本综述仍提供了若干重要启示。总体而言,脑脊液淀粉样蛋白相关标志物在现有研究中表现出最为一致的信号,并在生物学机制上具有较强的合理性,是潜在的风险分层候选指标。然而,根据GRADE评价结果,其证据质量仅为低至极低水平,因此相关结论应谨慎解读,更应视为探索性及假设生成性证据,而非可直接用于常规临床实践的确定性预测指标。
与此同时,多标志物炎症特征作为一种新兴方向,具有良好的发展前景,可能有助于更精细地刻画个体对术后认知功能下降的易感性。未来研究应着重开展大规模、多中心研究,在统一POCD定义及标准化生物标志物检测方法的基础上,对现有发现进行验证,并建立具有临床意义的阈值标准,从而推动围手术期认知风险分层的实际应用。
5. 结论(Conclusion)
现有证据表明,部分术前蛋白质生物标志物可能与大型骨科手术后发生的认知功能下降相关。然而,鉴于目前研究数量有限、异质性较高且证据质量较低,这些发现应主要视为假设生成性证据,其在其他高风险手术人群中的预测性能仍有待进一步验证。
在已研究的标志物中,淀粉样蛋白相关指标——尤其是脑脊液Aβ₁₋₄₂水平降低及Aβ/tau比值下降——在预测术后认知功能下降方面表现出最为一致且较强的关联性。尽管脑脊液淀粉样蛋白标志物在机制层面具有较高解释力,但基于血清的多标志物组合策略在临床转化方面可能更具可行性。相比之下,单一血清生物标志物(包括S100B、炎症细胞因子及神经损伤标志物)结果不一致,其变化更可能反映围手术期神经炎症反应,而非基础风险状态。
新兴证据提示,多标志物炎症特征可能具有进一步研究价值,但目前相关数据仍处于初步阶段。尽管这些发现具有一定前景,不同研究在生物标志物检测方法、认知评估方案及POCD定义方面存在显著差异,限制了结果的直接比较及临床应用转化。在解读上述结果时,应充分考虑现有研究中的临床异质性及潜在残余混杂因素的影响。
总体而言,本综述强调了术前淀粉样蛋白相关标志物及复合炎症特征在围手术期认知风险分层中的潜在价值。未来仍需开展大规模、多中心前瞻性研究,在统一认知结局定义、严格控制混杂因素及标准化生物标志物检测方法的基础上,对上述关联进行验证,并明确其是否具有临床意义上的预测价值。
此外,未来研究还应在不同类型手术背景下对这些生物标志物进行评估,以明确神经退行性易感性及炎症反应倾向在不同围手术期应激模式中的预测一致性。
原始文献:
Alwesabi AK, Gao B, Ma Y, et al. Toward precision risk stratification of postoperative cognitive dysfunction: Preoperative inflammatory and neurodegenerative protein biomarkers in orthopedic surgery: A systematic review. J Clin Anesth. 2026 Apr 16;112:112204.


