Cell Mol Immunol 山东大学齐鲁医院张铭湘团队揭示巨噬细胞ILF3在心肌梗死中的重要作用
时间:2026-05-08 20:02:38 热度:37.1℃ 作者:网络
急性心肌梗死(AMI)引起的缺血性心脏病是导致死亡最严重的心血管疾病之一,对AMI病理过程中的特异性靶点的研究以及新的治疗策略的开发尤为迫切。巨噬细胞介导的炎症反应在AMI中发挥重要作用。白细胞介素增强子结合因子3 (ILF3)是一种RNA结合蛋白,与心血管疾病以及炎症性疾病密切相关。然而,ILF3在心肌梗死中的作用及机制尚缺乏研究。
2026年4月22日,山东大学齐鲁医院心内科、络病理论创新转化全国重点实验室张铭湘教授团队在Cellular & Molecular Immunology期刊在线发表题为“Interleukin enhancer binding factor 3 exacerbates cardiac inflammation and injury following myocardial infarction by inhibiting Lys48-linked ubiquitination on HNRNPA2B1 in macrophages”的研究论文。该研究首次揭示了巨噬细胞ILF3在心肌梗死中的重要作用,发现巨噬细胞ILF3通过与HNRNPA2B1直接结合,并抑制其泛素化降解,两者形成复合物上调MAPK通路中Irak4的表达,进而加剧炎症反应,促进AMI后的心肌损伤。

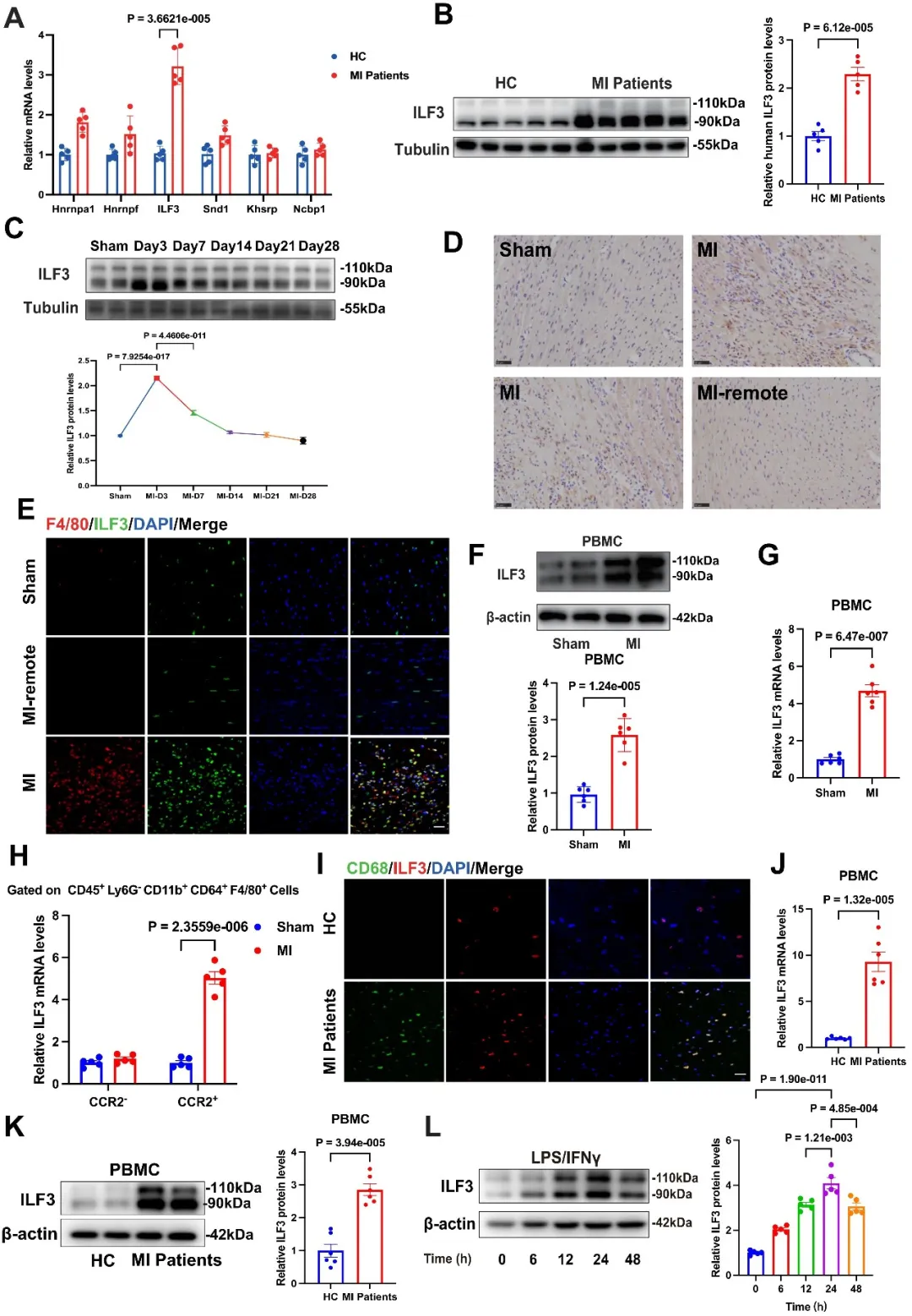
研究人员首先通过生物信息学分析以及对AMI人体心脏标本的分析发现,ILF3在梗死区心脏组织中表达升高。在对心梗小鼠不同时间节点心脏组织的实验分析发现,ILF3主要在心梗后3天显著升高,提示ILF3可能参与AMI急性期炎症反应。通过对AMI患者以及心梗小鼠外周血单核细胞的检测以及心梗组织免疫荧光染色分析发现,ILF3升高主要位于巨噬细胞中。
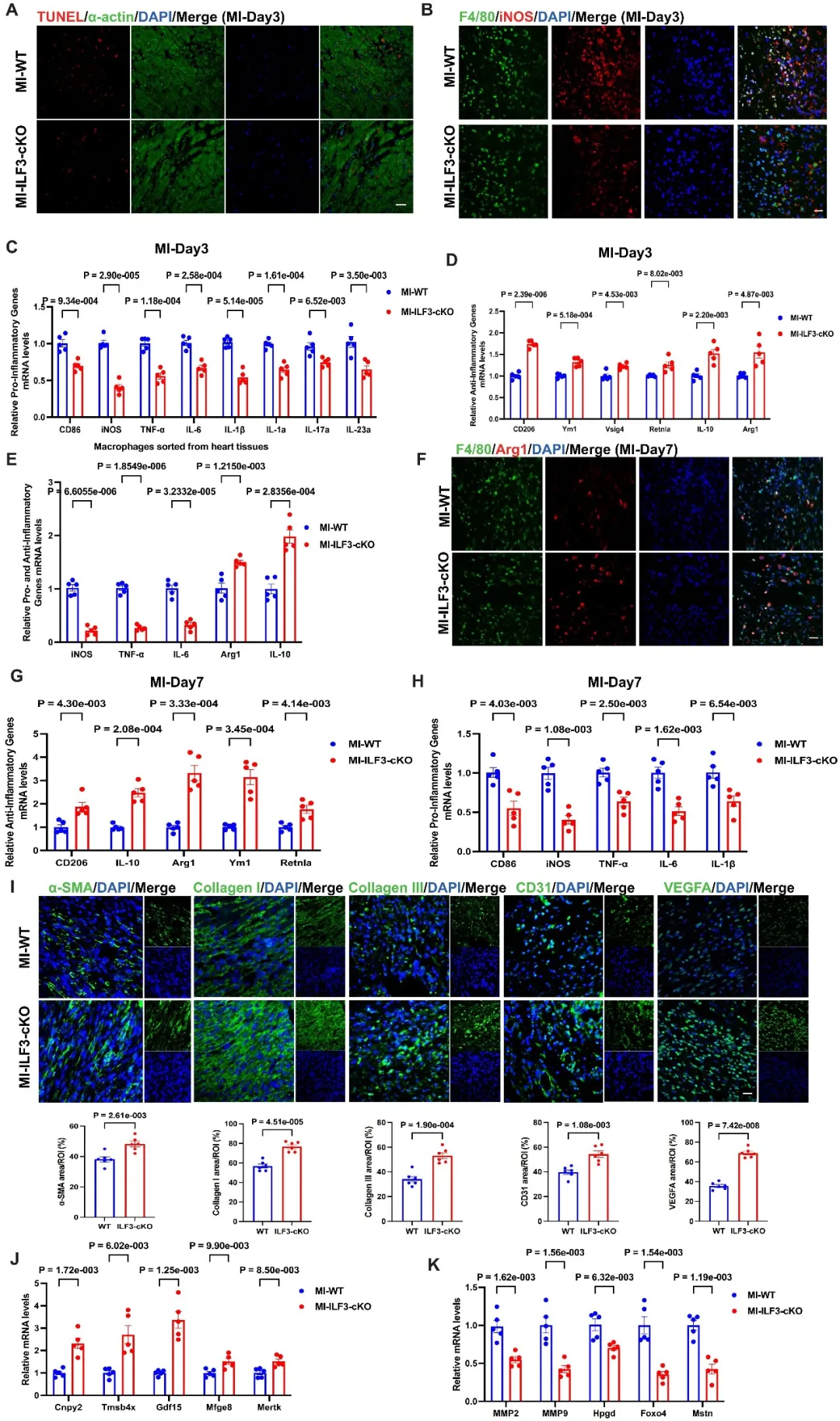
接下来,研究人员构建了巨噬细胞ILF3特异性敲除小鼠(ILF3-cKO), 并诱导AMI小鼠模型,发现ILF3-cKO显著改善了小鼠AMI后的心功能,并伴随较小的梗死面积和更高的存活率。同时,在AMI的早期炎症阶段,ILF3-cKO的心梗小鼠心脏组织中促炎因子表达水平降低, 而抗炎因子水平升高;在AMI后期增殖修复阶段,ILF3-cKO心梗小鼠具有更高水平的抗炎因子,同时伴随更加充分的心肌修复能力。这些发现表明,ILF3-cKO能够有效抑制AMI早期的过度炎症反应,并促进抗炎表型的转化,进而有利于AMI后的心肌损伤修复。
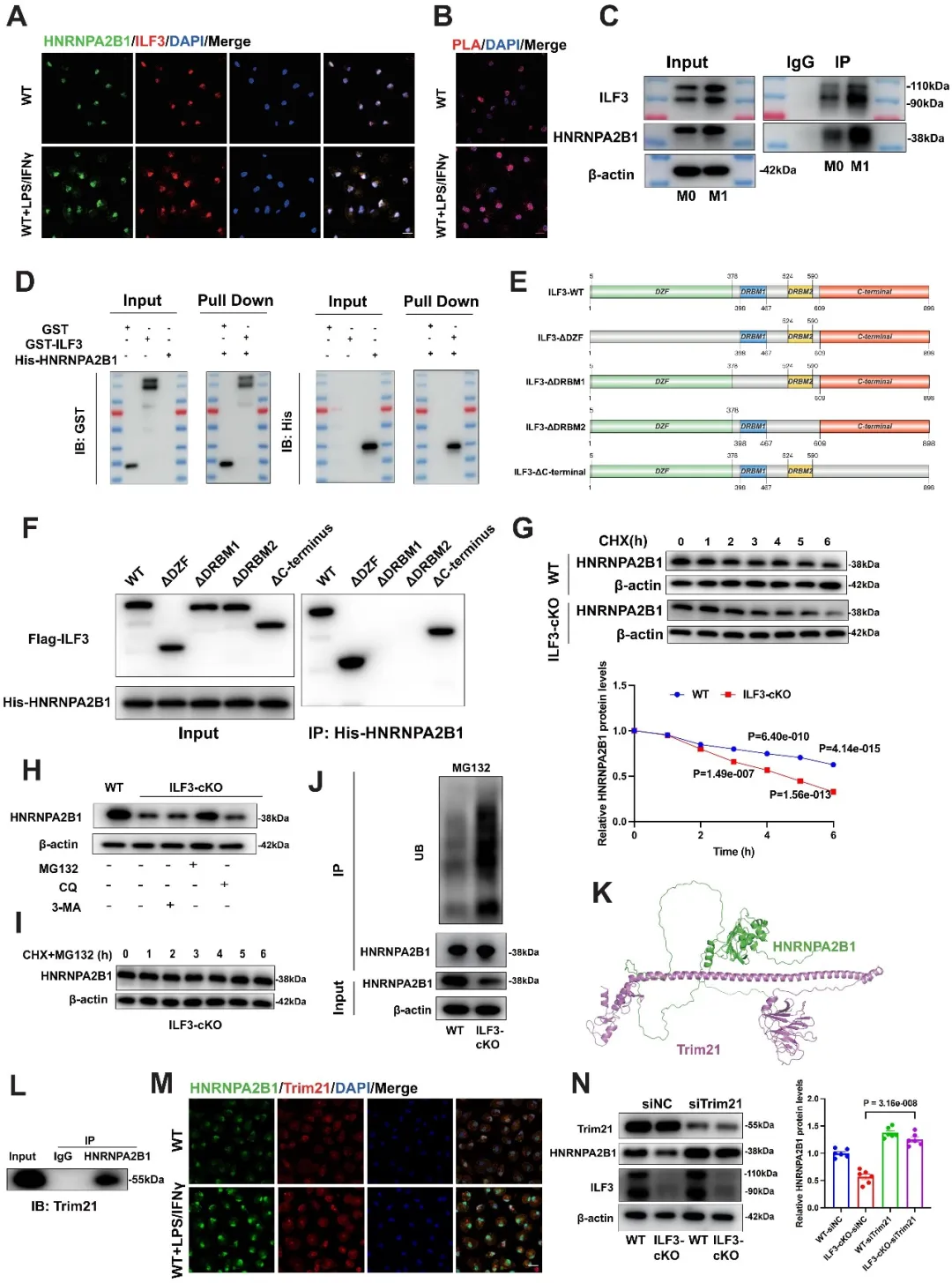
为了进一步探索巨噬细胞ILF3对AMI炎症过程的调控机制,研究人员对小鼠骨髓细胞进行了蛋白质组学测序以及IP-MS检测,发现ILF3直接与HNRNPA2B1结合并抑制E3泛素连接酶Trim21介导的HNRNPA2B1 K112位点的泛素化降解,从而维持HNRNPA2B1的蛋白稳定性,并形成ILF3/HNRNPA2B1复合物。KEGG分析发现,MAPK信号通路是ILF3/HNRNPA2B1复合物发挥调控作用的潜在富集通路,RIP/MeRIP等实验验证ILF3/HNRNPA2B1复合物可以与MAPK信号通路中的关键调控因子Irak4的mRNA结合并维持其稳定性,进而促进下游c-Jun/c-Fos通路的激活,放大AMI后心肌的炎症反应,加剧心肌损伤。ILF3-cKO则显著逆转了这一重要调控过程,从而抑制了炎症反应,促进AMI后的心肌修复。
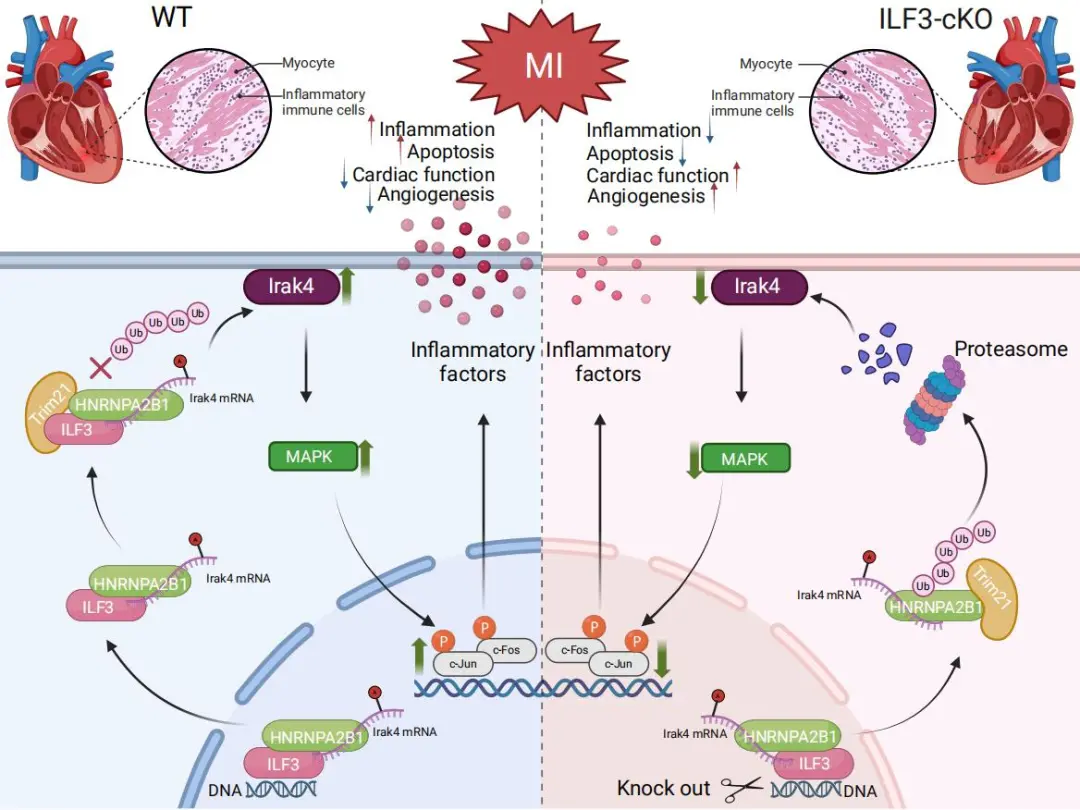
综上所述,本研究首次证实了巨噬细胞ILF3在心肌梗死中的重要调控作用,并发现ILF3主要通过与HNRNPA2B1结合进而调控炎症反应来参与心肌梗死的病理过程。具体机制而言,ILF3与HNRNPA2B1结合,阻止其被Trim21介导的泛素化降解,形成ILF3/HNRNPA2B1复合物从而稳定HNRNPA2B1。ILF3/HNRNPA2B1轴通过稳定Irak4的mRNA,激活c-Jun/c-Fos通路,放大炎症反应,加剧了AMI后的心肌损伤。本研究揭示了AMI后巨噬细胞调控炎症反应促进心肌损伤的新机制,为AMI的治疗提供新的理论依据和潜在的治疗靶点。
山东大学齐鲁医院心内科博士生张旭为该论文第一作者,山东大学齐鲁医院心内科张铭湘教授、中国科学技术大学第一附属医院心外科赵智伟教授、首都医科大学附属北京安贞医院赵远斐教授、山东大学齐鲁医院心内科王颖教授为该论文的通讯作者。该研究工作获得国家自然科学基金、山东省自然科学基金等项目资助。
原文链接:
https://www.nature.com/articles/s41423-026-01417-8


