【Blood】全文翻译:How I treat浆细胞白血病
时间:2026-05-08 20:22:33 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
浆细胞白血病(plasma cell leukemia,PCL)是一种少见且侵袭性极高的浆细胞恶性肿瘤,临床进展迅速,预后极差。《Blood》近日发表综述,阐述了PCL的特征、预后和治疗。

摘要
浆细胞白血病(PCL)是一种极具侵袭性的浆细胞恶性肿瘤,根据国际骨髓瘤工作组(IMWG)共识,定义为外周血中循环浆细胞≥5%且其他方面符合多发性骨髓瘤(MM)诊断标准的患者。这种超高危疾病具有独特的临床特征,包括频繁的髓外受累、严重血细胞减少、高钙血症、肾功能不全,和/或显著升高的β2-微球蛋白和乳酸脱氢酶水平。
PCL的分子特征包括高危细胞遗传学异常和突变,这些异常通过失调的黏附分子和趋化因子受体表达,促进加速增殖、凋亡抵抗、免疫逃逸以及骨髓微环境独立性。尽管自体干细胞移植、蛋白酶体抑制剂、免疫调节药物和单克隆抗体改善了历史预后,治疗范式仍在不断演变。新型治疗方法包括B细胞成熟抗原(BCMA)导向治疗(双特异性抗体和嵌合抗原受体T细胞疗法)、GPRC5D靶向治疗以及BCL-2抑制剂,在治疗原发性和继发性PCL方面显示出前景。尽管取得这些进展,PCL仍然研究不足,治疗方法主要从排除PCL患者的MM试验中外推而来。
本综述综合了现有证据,并通过临床病例展示实际治疗方法,同时强调了需要专门的前瞻性临床试验来有意义地改善这种挑战性疾病的预后。
引言
浆细胞白血病(PCL)是浆细胞恶液质最具侵袭性的形式,其特征为外周血中克隆性浆细胞负荷升高。PCL分为原发性(pPCL),即初发且无既往多发性骨髓瘤(MM)证据的患者;以及继发性(sPCL),即复发或难治性MM的白血病转化。约60-70%的PCL病例为原发性,其余30-40%为继发性。然而随着MM预后的改善,继发性PCL的病例有所增加。
PCL的诊断标准自1974年Kyle建立以来已发生显著演变,当时要求外周血循环浆细胞>20%且绝对计数>2×10⁹/L。回顾性研究检验了各种循环浆细胞阈值的预后影响,显示循环浆细胞≥5%的患者在临床结局和疾病特征方面与传统PCL标准患者惊人相似。因此国际骨髓瘤工作组(IMWG)于2021年修订了诊断标准,确立pPCL应定义为外周血循环浆细胞≥5%且其他方面符合MM诊断标准的患者。
循环肿瘤细胞(CTC)水平具有连续的不良预后意义,相关阈值低至≥2%的CTC即表现出与髓内浆细胞不同的分子特征,包括使骨髓独立性丧失的黏附分子缺失,以及促进外周循环和髓外扩散的趋化因子受体表达改变。
尽管治疗取得进展,PCL预后仍然不佳,传统化疗的历史中位总生存期(OS)仅7个月。近期多中心数据显示,pPCL的中位OS为36.6个月,sPCL仅3.2个月;接受自体干细胞移植(ASCT)的患者在两种亚型中均有显著改善的预后(pPCL:49.5个月 vs. 12.5个月;sPCL:16个月 vs. 3.4个月)。
本综述了审视PCL生物学、临床表现和治疗策略的当前认识,重点强调了新兴治疗范式以及在该超高危疾病中进行专门临床试验的关键需求。
病例1:最初拒绝常规化疗的年轻pPCL患者
一名50岁男性因乏力和背痛就诊。实验室检查显示血红蛋白(Hgb)9.2 g/dL,肌酐(Cr)1.4 mg/dL,IgG κ M蛋白4.5 g/dL,β2-微球蛋白(β2M)5.2 mg/L。骨髓(BM)活检显示70%非典型浆细胞。外周血显示4.5×10⁹/L循环浆细胞,占白细胞分类计数的22%。荧光原位杂交(FISH)报告del(17p)、dup1q和t(4;14)。弥散加权磁共振成像(DWI)显示多发溶骨性病变。诊断为原发性浆细胞白血病。
他接受达雷妥尤单抗-卡非佐米-来那度胺-地塞米松(Dara-KRd)治疗8个周期,达到非常好的部分缓解(VGPR)。尽管具有高危特征并建议进行ASCT,患者拒绝一线移植,但进行了干细胞采集和冷冻保存。他继续Dara-KRd治疗6个额外周期,然后转为KRd维持治疗。14个月后出现复发疾病。硼替佐米-泊马度胺-地塞米松(VPd)挽救治疗无反应。鉴于难治性疾病,他接受大剂量美法仑(MEL200)预处理ASCT 。
ASCT后第60天,他出现进展和新发髓外病变。他接受嵌合抗原受体(CAR)T细胞治疗评估,并进行白细胞分离术用于ciltacabtagene autoleucel(cilta-cel)制备。在6周制备期间,他接受一周期硼替佐米-地塞米松-顺铂-多柔比星-环磷酰胺-依托泊苷(VD-PACE)作为桥接化疗。随后接受cilta-cel输注,出现1级细胞因子释放综合征(CRS),使用托珠单抗管理,无免疫效应细胞相关神经毒性综合征(ICANS)。
患者反应迅速,第4周M蛋白不可测,1个月达到严格意义的完全缓解(sCR)。第3个月骨髓显示通过二代流式细胞术(NGF)检测的可测量残留病(MRD)阴性状态,敏感性10⁻⁵。输注后9个月仍处于持续sCR伴MRD阴性状态,需要每月静脉免疫球蛋白(IVIG)。
本病例说明了pPCL管理的几个关键点。虽然鉴于早期ASCT在pPCL中的显著生存获益,通常不建议推迟移植,但患者偏好可能并不总是与医疗建议一致。早期干细胞采集保留了移植选择,尽管最初推迟。CAR T细胞治疗后早期ASCT复发伴高危细胞遗传学的情况下,快速、深度的MRD阴性反应展示了BCMA CAR T细胞疗法的独特疗效,即使在既往治疗耐药的侵袭性pPCL中也是如此。尽管初始CAR T反应良好,持续监测至关重要,鉴于PCL的高复发风险。虽然在该高危情况下讨论了BCMA双特异性抗体(BsAb)维持治疗,但患者拒绝。
浆细胞白血病的病理生物学
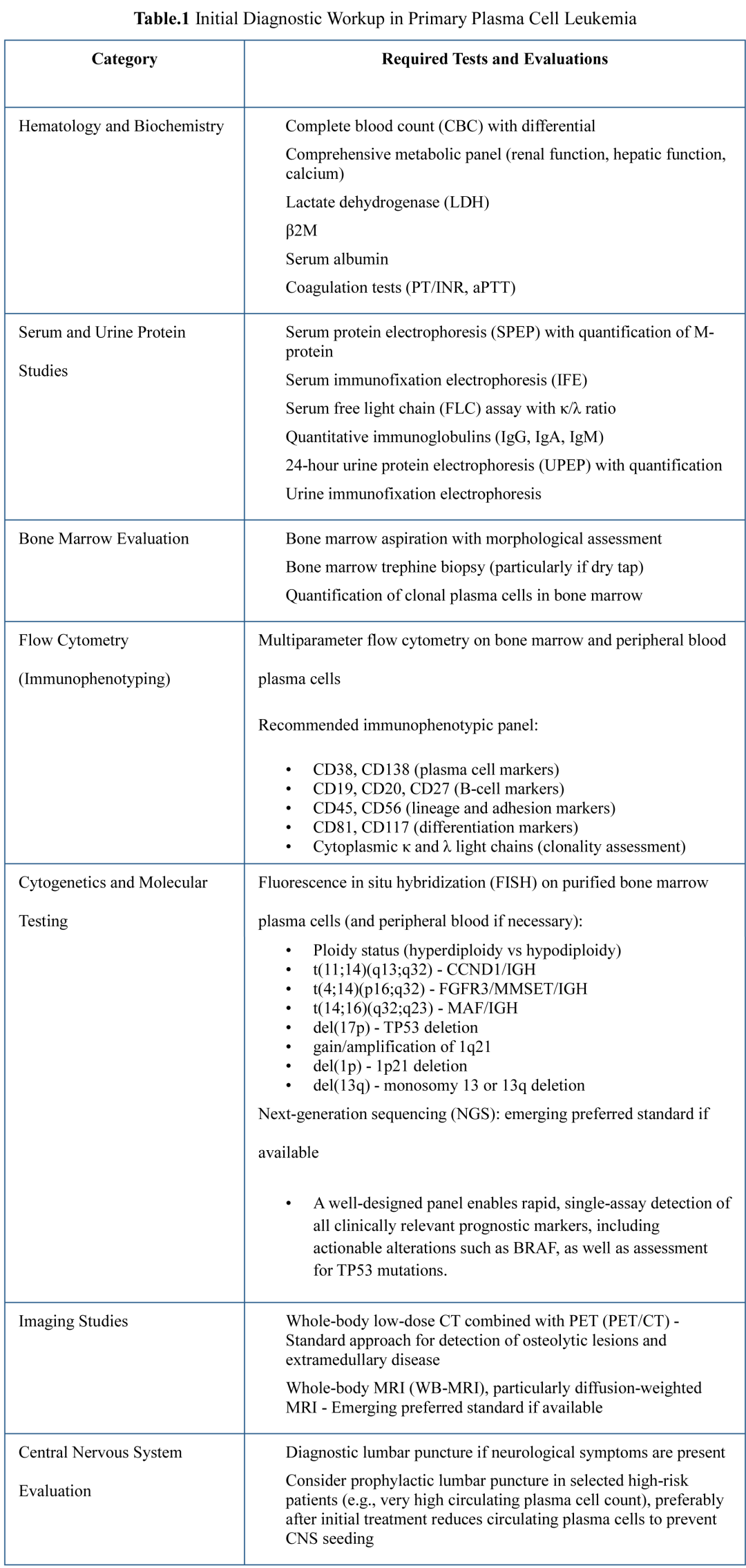
PCL的病理生物学涉及遗传畸变、表观遗传修饰、黏附分子表达改变、免疫逃逸机制以及骨髓微环境独立性的复杂相互作用(图1)。建议对所有pPCL患者进行以下检测(表1)。
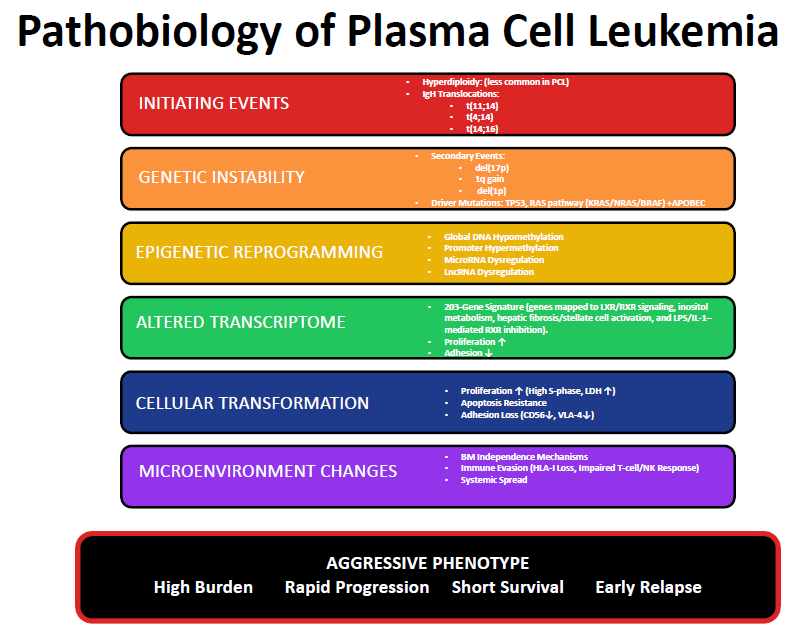
图1.浆细胞白血病的病理生理学
临床表现
与MM患者(中位年龄66-70岁)相比,pPCL患者通常就诊时年龄较轻(中位年龄60-64岁),但诊断时体能状态显著较差。临床表现可反映更高的肿瘤负荷和更具侵袭性的疾病生物学,pPCL患者更频繁地表现为严重贫血、血小板减少、高钙血症和肾功能损害。与新诊断MM相比,pPCL患者疾病负荷更大,高钙血症(24% vs 6%)和肾衰竭(25% vs 3%)的发生率更高。实验室参数可反映侵袭性疾病,β2M显著升高,乳酸脱氢酶(LDH)显著增加。髓外病变(EMD)是一个特别重要的鉴别特征,发生于20-34%的pPCL患者,而新诊断MM患者仅5-10%。sPCL的EMD发生率甚至高于pPCL。
外周血检查通常显示高达67%的病例呈白细胞-幼红细胞反应,循环浆细胞形态多变,从成熟样细胞到未成熟浆母细胞,常伴双核形式、Russell小体(胞质免疫球蛋白包涵体)和Dutcher小体(核内包涵体)。图2显示了浆细胞白血病的外周血形态。
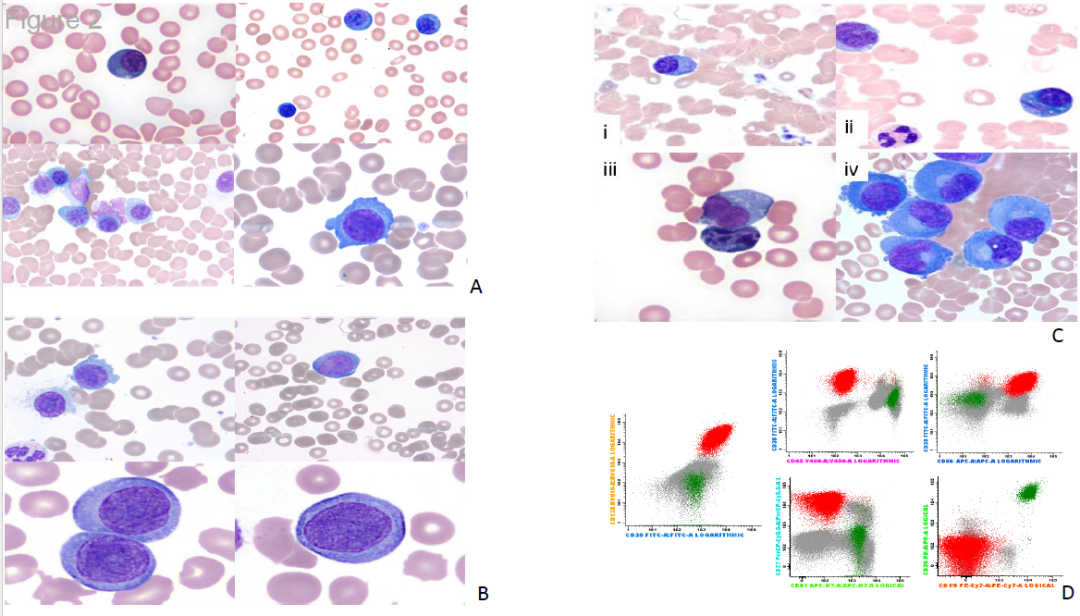
图2.浆细胞白血病外周血形态。(A)显示循环浆细胞形态异质性的复合图。细胞表现出典型的浆细胞特征,包括具有成团染色质的偏心细胞核、核周 hof和嗜碱性细胞质。注意单个细胞间核质比和染色质凝集程度的变化。(B)循环浆母细胞复合组。与成熟浆细胞相比,这些细胞表现出不成熟特征,染色质凝聚较少,核仁较明显,核质比较高。这些细胞表现出侵袭性浆细胞肿瘤的浆母细胞形态特征。(C)浆细胞白血病的代表性形态学变体。(i-ii)循环分泌 IgA的浆细胞(“火焰细胞”)由于 IgA积聚而表现出特征性的明亮的嗜酸性或火焰色细胞质。(iii)显示多核的双核浆细胞,浆细胞病的共同特征。(iv)循环浆母细胞伴细胞质泡,表明主动膜重塑和细胞应激或迁移的潜在标志物。(D)与背景 B细胞(绿色)相比,白血病浆细胞的免疫表型分析(用红色突出显示)。白血病浆细胞的CD138、CD38、CD56和 CD27呈阳性,而CD45、CD19和 CD81呈阴性。细胞也为 CD20阴性(未显示)。
PCL的骨骼受累与MM表现不同,广泛溶骨性病变发生率较低(59% vs. 81%),可能反映了白血病浆细胞与骨髓微环境相互作用的减少。中枢神经系统受累虽然罕见,但在PCL中比MM更常见,与极差预后相关,需要考虑在高危患者中进行预防性鞘内治疗。
生物学特征
与MM中约50%存在超二倍体且通常预后良好不同,超二倍体在pPCL中仅存在0-8.8%,以低二倍体和非超二倍体核型为主。pPCL显示不良细胞遗传学特征频率显著高于新诊断MM,包括高危FISH异常(47% vs 18%)、IgH易位(49% vs 26%)、del1p32(35% vs 10%)、del17p13(39% vs 10%)和t(11;14)(50% vs 19%)。多种分子异常常可同时发生。重要的是,尽管共享del(17p),但pPCL和新诊断MM表现出不同的转录组谱,超过3500个差异表达基因以及RNA剪接机制的显著差异,从而强调了细胞遗传学一致性并不意味着这两种疾病之间的生物学等同。
t(11;14)易位可导致CCND1失调,在pPCL中显著普遍,发生于39%的患者,使其成为最常见的IgH易位。t(11;14)亚群可能代表pPCL内一个独特的生物学亚组,具有有利的预后影响,但当与高危异常共存时这种有利性被显著抵消。在一项比较pPCL和sPCL的回顾性研究中,1q21增益/扩增(1q21+)被确定为sPCL中最常见的细胞遗传学发现,存在于75%的患者中。
蛋白质组学分析已鉴定pPCL中CRIP1和CRIP2上调,而在MM队列中鉴定的"PCL样"转录特征强化了PCL生物学沿连续体存在而非二元实体的概念。值得注意的是,在较大MM队列中已鉴定出"PCL样"转录特征,从而定义了共享pPCL分子特征的高危亚群,尽管未达到循环浆细胞阈值。这也强化了PCL生物学沿连续体而非二元实体存在的概念。
在对参加Total Therapy方案的1474例患者的综合分析中,细胞遗传学异常在pPCL患者中显著过高(81% vs. 非pPCL的32%,P<0.001)。低二倍体在pPCL中占48%,而非pPCL患者占12%(P<0.001)。基因表达谱分析显示pPCL样本形成与非pPCL不同的紧密、均匀聚类,在CD-1和MF分子亚组中过度代表——两者均与高危疾病相关。重要的是,203个差异表达基因探针区分pPCL与非pPCL,通路分析鉴定出脂质代谢通路相关基因的富集,包括LXR/RXR激活和肝星状细胞激活。
除细胞遗传学异常外,pPCL的特征还在于驱动基因组不稳定性和侵袭性行为的独特突变谱。TP53突变发生于约20-30%的pPCL病例,显著高于新诊断MM,与特别差的预后相关。RAS通路突变(KRAS、NRAS和BRAF)频繁发生,KRAS突变在高达40%的病例中检测到,促进增强的增殖和存活信号。值得注意的是,在部分pPCL病例中可观察到APOBEC突变活性,可能在某些易位背景下富集(如MAF驱动疾病),促进受影响病例的基因组不稳定性和克隆演化;然而这一特征并非PCL的普遍特征,不应过度泛化。这种突变负荷伴随着深刻的表观遗传重编程,包括全局DNA低甲基化以及影响肿瘤抑制基因的启动子特异性高甲基化。MicroRNA谱分析揭示pPCL与MM相比的独特失调模式,miR-15a/16-1簇下调和致癌miRNA过表达促进侵袭性表型。
pPCL的细胞表型可反映其侵袭性生物学行为,特征为显著升高的增殖活性,高S期分数(常>3%)和升高的LDH水平,与通常静止的骨髓驻留骨髓瘤细胞形成鲜明对比。pPCL的一个定义特征为黏附分子表达的丧失,特别是70-80%病例中CD56(NCAM)下调和VLA-4(CD49d)表达减少,从而促进从骨髓微环境脱离并支持不依赖基质支持的自主生长。这种骨髓依赖性丧失,加上通过BCL-2家族蛋白失调和存活通路激活导致的凋亡抵抗,使恶性浆细胞能够在无外周循环中存活和增殖,无需保护性骨髓微环境。自主生长能力和改变的细胞因子依赖模式将pPCL与MM区分开来,后者的恶性细胞在很大程度上仍依赖骨髓基质细胞相互作用。
免疫逃逸机制在pPCL发病机制中发挥关键作用,并促进其侵袭性临床病程。这些免疫缺陷,加上pPCL特征性的复杂结构改变、高突变负荷(包括t(11;14)患者中特别高的双等位基因TP53失活率)和表观遗传失调,创造了允许快速疾病进展和早期治疗抵抗的环境,最终导致这种侵袭性疾病相关的极差预后。
预后模型
PCL的预后仍然不佳。一项多中心研究开发了风险分层模型,鉴定年龄≥60岁、血小板计数≤100×10⁹/L和外周浆细胞计数≥20×10⁹/L为独立不良预测因子,中位生存期从无风险因素患者的46个月到具有两个或三个因素患者的仅12个月不等。
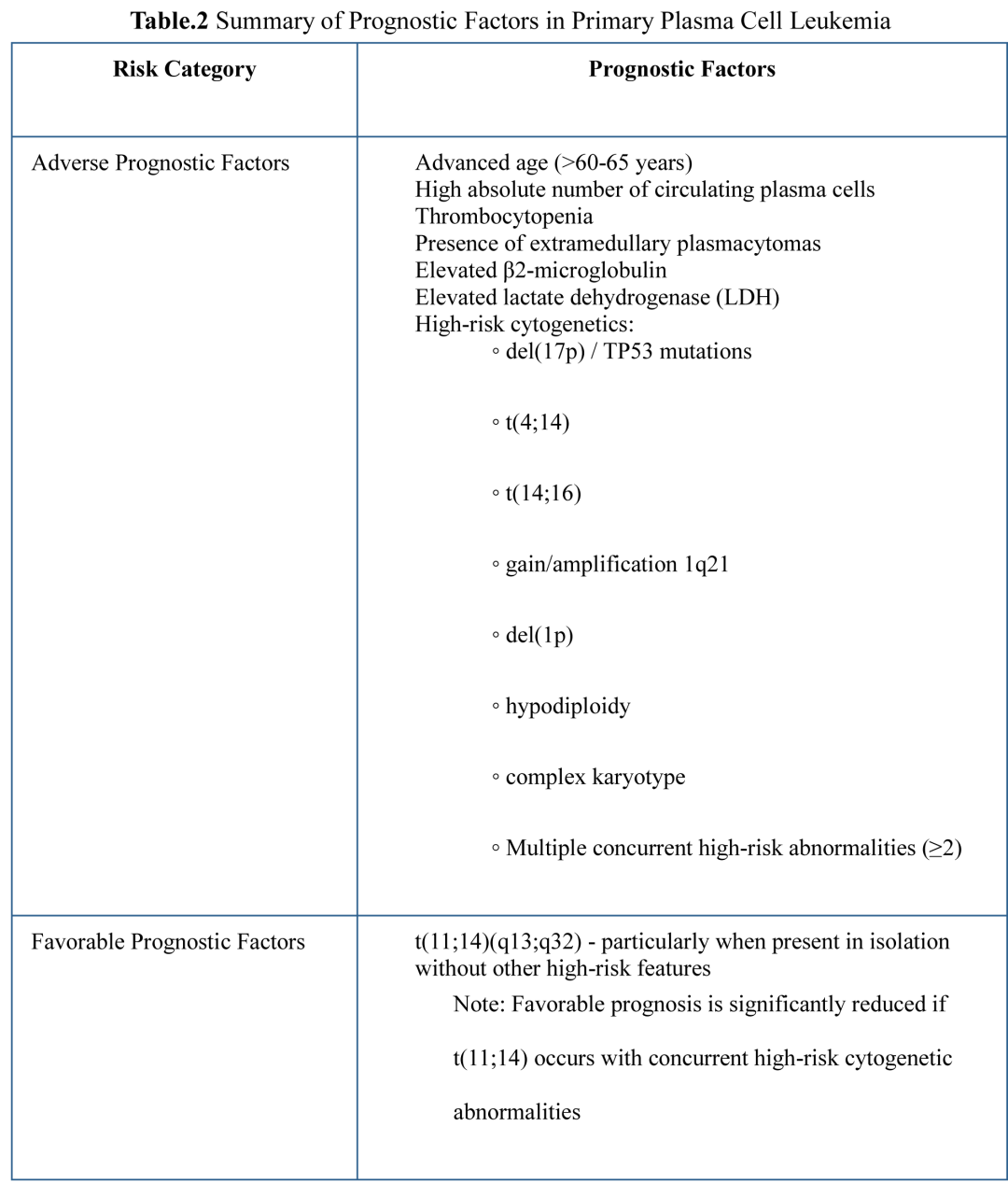
然而,新兴数据表明分子异质性也可能影响结局,无并发高危特征的孤立t(11;14)原发性PCL似乎预后较好(中位OS 39个月 vs. 18个月),而非t(11;14)原发性PCL特征为双等位基因TP53改变、独特的IRF4突变和不同的转录组谱,强调需要纳入特定遗传谱的精细预后模型(表2)。sPCL比pPCL预后更差,历史中位生存期仅2-7个月,反映了侵袭性白血病转化和既往多药暴露导致的治疗抵抗。
病例2:适合强化化疗的老年pPCL患者
一名72岁女性因进行性乏力和背痛加重就诊。实验室检查显示Hgb 9.2 g/dL,白细胞(WBC)3.4×10⁹/L,血小板53×10⁹/L,Cr 1.0 mg/dL,白蛋白3.5 g/dL,钙8.4 mg/dL。血清蛋白电泳(SPEP)显示无单克隆蛋白,血清游离轻链水平正常。骨髓活检显示69%非典型浆细胞。外周血显示12%循环浆细胞。FISH显示del(13q)和t(11;14)。诊断为pPCL。
她最初在当地接受一周期Dara-Rd治疗无反应,转至我院。随后接受2周期VD-PACE治疗达到部分缓解(PR)。缓解后,她接受串联ASCT,两次移植均采用MEL200预处理。移植后超过1年,她在来那度胺、硼替佐米、地塞米松(RVD)维持治疗下保持缓解。首次复发时,她接受卡非佐米、泊马度胺、地塞米松(KPd)治疗达到PR。第二次复发时,她接受基于维奈克拉的治疗,初始有反应随后进展。她随后发展为sPCL,并先后进展于特立妥单抗和塔奎妥单抗,两者均提供不到3个月的短暂疾病控制。
该患者接受CAR T细胞治疗评估。她进行白细胞分离术用于cilta-cel制备,并在制备期间接受桥接化疗。cilta-cel输注后,她最初显示疾病反应。然而,输注后第40天,白血病期疾病复发,表现为sPCL,尽管自初始pPCL诊断以来已实现超过3年的髓内疾病控制。尽管给予支持治疗,她于cilta-cel后第40天死于进展性疾病。自初始pPCL诊断以来的OS超过3年。
本病例说明了初始疾病生物学如何支配长期结局,尽管通过多种治疗实现深度缓解。虽然VD-PACE后串联ASCT提供超过1年的缓解,但随后各线治疗复发频率增加、缓解持续时间逐渐缩短的模式(包括新型药物、BsAbs,最终CAR T细胞疗法)反映了其疾病的固有侵袭性。本病例强调,尽管有多种有效治疗方式可用,但初始疾病特征可以预测最终结局,并强调了在该高危人群中需要新方法。
原发性浆细胞白血病的管理
治疗前评估和支持治疗
全面的治疗前评估和积极的支持治疗对成功的PCL管理至关重要(图3)。

图3.治疗前评估和支持治疗
完成诊断检测(表1)后,应使用IMWG虚弱评分和体能状态标准评估患者体能,以确定包括ASCT在内的强化治疗资格。诊断确认后应迅速开始治疗。支持治疗干预必须立即实施,特别强调通过积极静脉补液和降尿酸预防肿瘤溶解综合征。大多数患者在初始治疗期间需要住院密切监测,以管理急性并发症,包括高钙血症、感染和血细胞减少。额外支持措施包括风险分层的血栓预防、抗微生物预防和每月骨改良药物的骨骼保护。
Fit患者
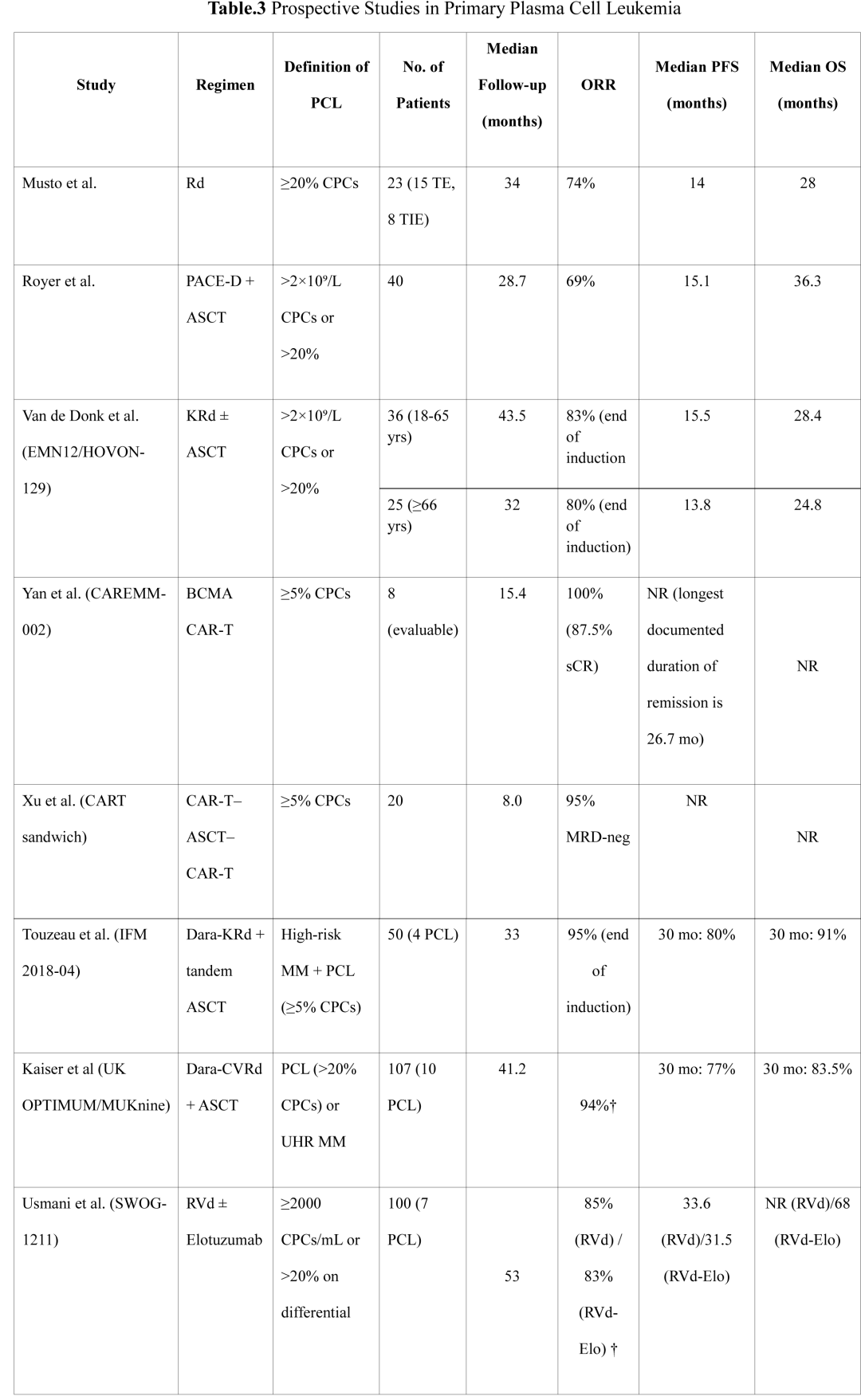
对于fit的pPCL患者,整合新型药物、ASCT和延长维持治疗的强化治疗方法已成为标准治疗,累积证据显示与历史系列相比生存结局有显著改善(图4;表3)。

图4.原发性浆细胞白血病的治疗
对无需立即住院的患者,建议使用四药方案诱导治疗4-6个周期。对于可能需要立即住院治疗的血细胞减少患者,推荐使用VD-PACE化疗1-2个周期进行细胞减灭,因为大多数pPCL患者就诊时伴有细胞减少,阻碍首个周期的标准门诊治疗。基于近期数据显示含抗CD38抗体方案优越结局,首选达雷妥尤单抗基础联合方案如达雷妥尤单抗、硼替佐米、来那度胺和地塞米松(D-VRd),或艾沙妥昔单抗基础四药方案。在可及情况下,优选使用卡非佐米替代硼替佐米,鉴于其在高危疾病中的优越疗效特征。
OPTIMUM试验专门评估了强化达雷妥尤单抗、环磷酰胺、硼替佐米、来那度胺和地塞米松(D-CVRd)五药方案在107例超高危骨髓瘤和pPCL患者(n=10)中的应用,显示30个月无进展生存期(PFS)为77%,中位PFS在超过3年随访后仍未达到。
诱导后,fit患者应在可行时进行串联ASCT,使用大剂量美法仑(200 mg/m²)预处理;否则,患者应在诱导治疗后至少进行单次ASCT。不建议推迟ASCT。欧洲骨髓瘤网络(EMN)EMN12/HOVON-129试验显示,在年轻患者(18-65岁)中该方法达到86%的总缓解率,50%达到完全缓解或更好。在20例评估MRD的患者中,80%达到MRD阴性。中位PFS为15.5个月,OS为28.4个月。另一项评估Dara-KRd诱导和巩固后串联ASCT的前瞻性研究纳入50例高危新诊断MM患者。3例pPCL患者中,1例在诱导期间早期疾病进展,另2例患者在维持期保持无进展,所有患者的30个月PFS和OS分别为80%和91%。大型回顾性分析也证实了ASCT在pPCL中的获益。国际血液和骨髓移植研究中心(CIBMTR)对97例患者的研究显示3年PFS和OS分别为34%和64%,治疗相关死亡率(5%)可接受。
延长巩固和维持治疗对于最大化缓解深度和延长缓解至关重要。建议ASCT后尽可能进行4个周期四药基础巩固治疗,随后持续维持治疗,使用来那度胺联合蛋白酶体抑制剂(优选卡非佐米)或抗CD38抗体,直至疾病进展或不可耐受毒性。该策略利用蛋白酶体抑制剂-来那度胺或抗CD38抗体-来那度胺联合方案的已证实的长期疗效进行持续疾病控制。重要的是,该方法保留了复发时的治疗选择:停用抗CD38抗体维持治疗且未出现难治性疾病的患者,可使用替代抗CD38抗体基础方案再治疗。
pPCL延长维持治疗的原理令人关注。EMN12/HOVON-129试验使用卡非佐米-来那度胺(KR)维持,年轻队列患者维持治疗中位26.6个月。该方法针对pPCL的基本生物学,其中MRD持续存在导致早期复发。达到MRD阴性(特别是在高危细胞遗传学中)与改善结局强烈相关,维持治疗提供了实现和维持该状态的最佳机会。
PCL中的MRD评估应结合骨髓评估(通过验证的高敏感性技术:NGF或二代测序[NGS],敏感性≥10⁻⁵)和功能影像学(PET-CT和弥散加权MRI),以检测骨髓取样无法捕捉的髓外疾病。模态选择应受当地实验室可用性和专业知识指导。鉴于pPCL快速早期进展的高风险,建议ASCT后尽早开始巩固/维持治疗,理想情况下第+60天(如果计数恢复充分)。
对于高度选择的年轻患者(<65岁),若有可用的匹配供者,自体ASCT后未达到完全缓解,且治疗选择有限,可考虑减低强度预处理异基因SCT。然而鉴于高治疗相关死亡率和PCL中移植物抗骨髓瘤获益的证据有限,通常不推荐异基因SCT,特别是当其他治疗可用时。
非fit患者
对于因高龄、合并症或虚弱而不适合强化治疗和/或ASCT的pPCL患者,治疗结局仍然具有挑战性,尽管新药的引入与历史系列传统化疗相比改善了生存。
在耐受情况下,建议使用四药方案延长诱导治疗8-12个周期。首选方案包括达雷妥尤单抗基础四药如D-VRd或艾沙妥昔单抗基础联合(IsaVRd)。对于无法耐受四药方案的患者,替代三药选择包括DRd(达雷妥尤单抗、来那度胺、地塞米松)、DVd(达雷妥尤单抗、硼替佐米、地塞米松)、KRd(卡非佐米、来那度胺、地塞米松)或VRd。EMN12/HOVON-129试验证明,KRd诱导后KR维持治疗的老年患者(≥66岁)达到中位PFS 13.8个月和OS 24.8个月,与既往回顾性系列相比生存翻倍。
诱导后,建议使用两药维持进行延长治疗直至疾病进展,联合硼替佐米或卡非佐米与来那度胺,或达雷妥尤单抗与来那度胺。选择取决于耐受性和患者相关因素,目标是在维持疾病控制的同时保留生活质量。对于无法耐受联合治疗的frail患者,可考虑单药维持使用来那度胺或达雷妥尤单抗。重要的是,建议避免单药延长治疗,除非患者无法耐受联合基础方法,因为双药维持在高危疾病中可提供优越的疾病控制。
应根据虚弱和器官功能实施剂量调整,管理细胞减少、神经病变和感染。Frail患者可能需要进一步减量和时间表调整,以在优化疾病控制的同时维持耐受性。
原发性难治性疾病
病例3:对一线常规化疗难治的pPCL
一名58岁男性表现为原发性难治性疾病。他出现背痛,发现T12骨折。实验室检查显示钙升高10.8,肌酐1.37。实验室检查显示Hgb 5.9 g/dL,WBC 7.78×10⁹/L,血小板13×10⁹/L,Cr 3.5mg/dL,钙10.8 mg/dL,白蛋白3.6 g/dL。SPEP显示κ轻链单克隆蛋白。血清游离轻链显示κ 67.5 mg/dL,λ 0.8 mg/dL,κ/λ比值81.5。骨髓活检显示95%浆细胞和超过22%循环浆细胞。诊断为pPCL。
他最初在不同机构接受2周期VD-PACE治疗,疾病进展,随后一周期D-VRd治疗无反应,转至我院。
他入院时复查骨髓显示100%浆细胞,FISH显示t(11;14)。他开始接受维奈克拉联合卡非佐米和地塞米松治疗,κ游离轻链水平改善。他进行环磷酰胺基础干细胞动员的干细胞采集,随后接受两次MEL200预处理的串联ASCT,达到MRD阴性。
鉴于其就诊时高度难治性疾病,他最初维持维奈克拉为基础方案,但因腹泻无法耐受。他开始特立妥单抗维持,每月持续使用达2年。系列骨髓活检确认整个治疗期间持续MRD阴性状态。特立妥单抗因反复感染停用,停药后12个月仍处于持续MRD阴性缓解。
本病例说明了管理原发性难治pPCL的关键原则。尽管初始对大剂量化疗和四药治疗耐药,基于维奈克拉的治疗实现细胞减灭, 强调了BCL-2抑制在t(11;14)侵袭性疾病中的潜力。串联ASCT达到MRD阴性证明,即使原发性难治pPCL,在初始细胞减灭后通过强化治疗也可控制。ASCT后特立妥单抗维持治疗是维持MRD阴性缓解的新策略,维持停药后12个月持续阴性提示使用新型免疫疗法在该挑战性人群中可能实现持久缓解。
鉴于pPCL特征性的侵袭性生物学和快速增殖,强烈建议尽早使用最强效可用治疗,而非序贯常规挽救方法。真实世界研究表明,虽然EMD和高危细胞遗传学(pPCL中常见)可能影响结局,但BCMA导向治疗(包括CAR-T治疗)仍保持高度活性。类似地,BCMA靶向BsAbs如特立妥单抗和GPRC5D靶向BsAbs如塔奎妥单抗已显示高单药活性,应在复发早期考虑。BsAbs的优势包括其即用可用性和快速启动潜力,无需CAR-T治疗相关的制备延迟,这在快速进展的pPCL中可能特别重要。
对于t(11;14)患者,基于维奈克拉的治疗可作为首次复发或初始反应不佳时的合理治疗选择。多个病例报告和小型系列显示,在携带t(11;14)的复发pPCL患者中,维奈克拉作为单药或联合地塞米松和达雷妥尤单抗,显示出令人印象深刻的反应。应在诊断时专门评估该易位的存在,以指导复发时的治疗选择。对于无法获得CAR-T、BsAbs或维奈克拉(t(11;14)病例)的患者,可考虑纳入前线未使用药物的挽救化疗联合方案,尽管反应往往短暂。鉴于该人群有效治疗的关键未满足需求,应强烈鼓励参加临床试验。
继发性浆细胞白血病的管理
sPCL的管理需要高度个体化的决策,仔细平衡疾病控制目标与生活质量、患者体能状态和个人价值观。与pPCL不同,pPCL中积极的一线治疗可实现延长缓解,sPCL患者已暴露于多线治疗,常累积治疗相关毒性、显著合并症和深刻的治疗抵抗。因此,方法必须个体化,考虑患者的治疗史、剩余治疗选择、体能状态、器官功能,最重要的是,患者的管理目标。
对于体能状态保留且既往治疗暴露有限的患者,使用既往未使用的新药进行细胞减灭方法可能提供症状控制和适度生存延长。T细胞重定向治疗(包括BCMA导向CAR-T或BsAbs)可作为未暴露于这些方式且器官功能充足的患者的最强效选择,但这些新型治疗在sPCL中的结局次优。对于t(11;14)患者,基于维奈克拉的联合方案可能提供有意义的反应。然而,临床医生必须认识到,sPCL中的缓解率和持续时间显著劣于早期复发/难治性骨髓瘤。
对于体能状态差、多线既往治疗暴露、显著器官功能障碍或尽管近期治疗仍快速疾病进展的患者,早期整合姑息治疗和关于舒适导向方法的讨论至关重要。sPCL管理的关键原则是,治疗决策不能遵循一刀切算法,而必须根据每位患者的独特临床情况、剩余治疗选择和个人目标量身定制。

图5.继发性浆细胞白血病的治疗
未来方向
PCL患者的未来充满希望,但实现这一潜力需要根本性的方法转变:专门的前瞻性试验、预防抗原逃逸的创新策略,以及PCL患者在临床研究中的系统纳入。PCL患者大多被排除在MM试验之外,使治疗决策依赖回顾性数据和专家意见。未来的MM试验应强制纳入PCL并进行预设亚组分析,应优先开展专门的前瞻性试验。值得前瞻性评估的关键策略包括:(1)ASCT后更早的免疫基础治疗(BsAbs或CAR-T)以实现持久MRD阴性;(2)MRD指导的治疗调整;以及(3)靶向BCL-2依赖性、免疫逃逸和基因组不稳定性的新型联合方案。持续的研究承诺对于开发这种罕见、高流失率疾病的循证框架至关重要。PCL治疗虚无主义的时代已经过去。随着现有有效药物的显著阵列和长期幸存者的存在证明持久疾病控制是可实现的,该领域既有工具也有责任为这种毁灭性疾病的患者转变结局。
参考文献
Blood . 2026 May 1:blood.2025032145. doi: 10.1182/blood.2025032145.


