福州大学/深圳先进院AM:开发动态共价肽-药物偶联物,应对阿尔茨海默病进展异质性
时间:2026-05-08 20:20:31 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
背景介绍
阿尔茨海默病(AD)是最常见的神经退行性疾病,影响着10-30%的老年人口。尽管近期FDA批准了三种靶向β-淀粉样蛋白(Aβ)聚集体的抗体药物,但其临床获益仍存在争议,且临床试验严格限定于轻度认知障碍或轻度痴呆患者。AD并非静态疾病,而是一个动态进展过程,个体间疾病进展存在显著异质性。基于静态或单一生化指标制定治疗方案,容易因用药错误导致治疗失败。虽然通过算法对AD人群进行精细分层在概念上可行,但这会增加治疗方案的复杂性、成本和诊疗负担。
研究思路
针对上述挑战,福州大学化学学院的杨黄浩教授、陈兆委教授与中国科学院深圳先进技术研究院生物医学与健康工程研究所的陈支通研究员团队合作,设计了一种基于动态共价苯硼酸酯键的肽-药物偶联物(CPKNAs)。该偶联物由Aβ结合肽(KLVFF)和姜黄素(Cur)通过可逆的苯硼酸酯键连接,可自组装形成约90 nm的纳米组装体。CPKNAs能够解码AD进展中三个关键生物标志物(Aβ、活性氧ROS和葡萄糖)的时空演变模式,通过动态共价键的水解、氧化分解和竞争性结合,实现分层次的自适应药物释放:在早期单一病理阶段释放少量Cur,在多种病理共存的中晚期释放更多Cur。通过七种细胞模型和三种不同AD阶段的转基因小鼠(3xTg、APP/PS1、5xFAD)验证,CPKNAs在统一给药方案下,能够根据病变严重程度自适应性调节脑内药物分布和剂量,有效减轻细胞损伤、改善脑功能障碍,且避免了传统游离姜黄素的“双相剂量-反应”问题。相关内容以Dynamic Covalent Peptide-Drug Conjugates Address the Heterogeneity in Alzheimer‘s Disease Progression为题,发表在Advanced Materials!

图片解析
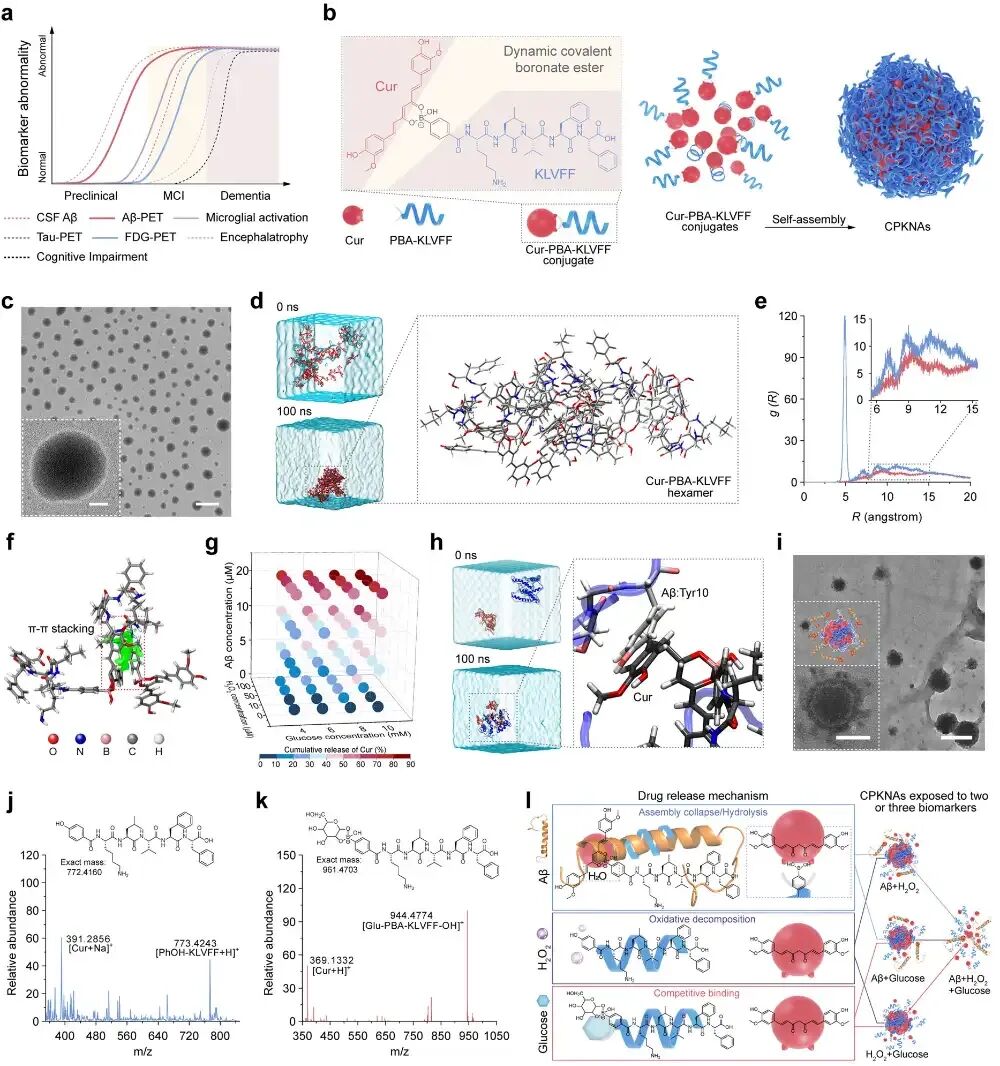
图1. 用于应对AD进展异质性的层次响应性治疗剂的设计: (a) AD病理进展的动态生物标志物模型,Aβ沉积、神经炎症和糖代谢障碍依次出现并最终共存。(b) 动态共价肽-药物偶联物(Cur-PBA-KLVFF)的分子结构及其自组装形成CPKNAs的示意图。(c) CPKNAs的TEM图像,标尺200 nm,插图为放大图像,标尺20 nm。(d) MD模拟显示Cur-PBA-KLVFF偶联物在水溶液中的初始和最终自组装状态。(e) 硼-硼原子(蓝线)和KLVFF羧基(红线)的径向分布函数(RDF)。(f) RDG等值面图(RDG=0.50),绿色表示Cur-PBA-KLVFF二聚体间的π-π堆积相互作用。(g) 在不同浓度Aβ₄₀肽、H₂O₂和葡萄糖存在下的Cur释放百分比,3D散点图展示多 biomarker协同效应。(h) MD模拟显示Cur-PBA-KLVFF五聚体与五个Aβ₄₀肽在模拟水盒中的相互作用,插图显示Tyr10残基通过π-π堆积插入疏水核心。(i) CPKNAs与Aβ₄₀肽(20 µM,2 h)孵育后的TEM图像,显示纳米组装体解体。(j) CPKNAs与H₂O₂(100 µM,8 h)孵育后的质谱图,显示氧化分解产物。(k) CPKNAs与葡萄糖(10 mM,24 h)孵育后的质谱图,显示竞争性结合产物。(l) CPKNAs在模拟病理条件下的层次响应释放机制示意图。
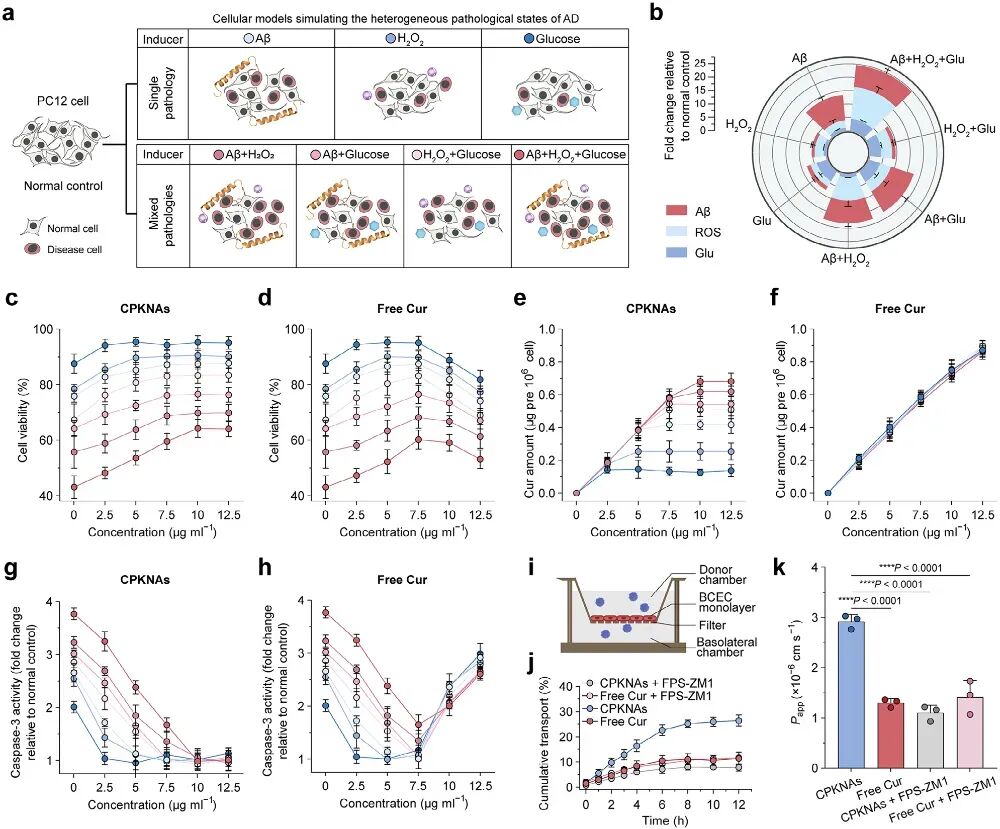
图2. CPKNAs治疗异质性AD病变的体外验证: (a) 七种细胞AD模型的建立示意图:分别用Aβ₄₀、H₂O₂、葡萄糖或其组合处理PC12细胞,模拟单一或混合病理。(b) 不同诱导剂处理PC12细胞中Aβ₄₀、ROS和葡萄糖水平相对于正常细胞的倍数变化。(c-d) 不同剂量CPKNAs(c)或等量游离Cur(d)处理后病变细胞的存活率:CPKNAs呈剂量依赖性挽救,平台值随病变严重程度递增;游离Cur呈双相曲线,低剂量有效、高剂量有毒。(e-f) 不同剂量CPKNAs(e)或游离Cur(f)处理6 h后病变细胞中Cur含量的定量:CPKNAs的细胞内Cur水平呈自限性,与初始病变严重程度正相关;游离Cur则剂量依赖性蓄积,与病变程度无关。(g-h) Caspase-3活性:CPKNAs处理组各剂量下caspase-3水平均低于未处理组;游离Cur在超过最佳阈值剂量后显著诱导caspase-3上调。(i) BCEC单层Transwell系统示意图。(j) 游离Cur(5 µg/mL)、CPKNAs(5 µg/mL)以及FPS-ZM1预处理后CPKNAs的跨BCEC单层累积转运量。(k) 表观渗透系数(P_app):CPKNAs约2.9×10⁻⁶ cm/s,是游离Cur的2.3倍。
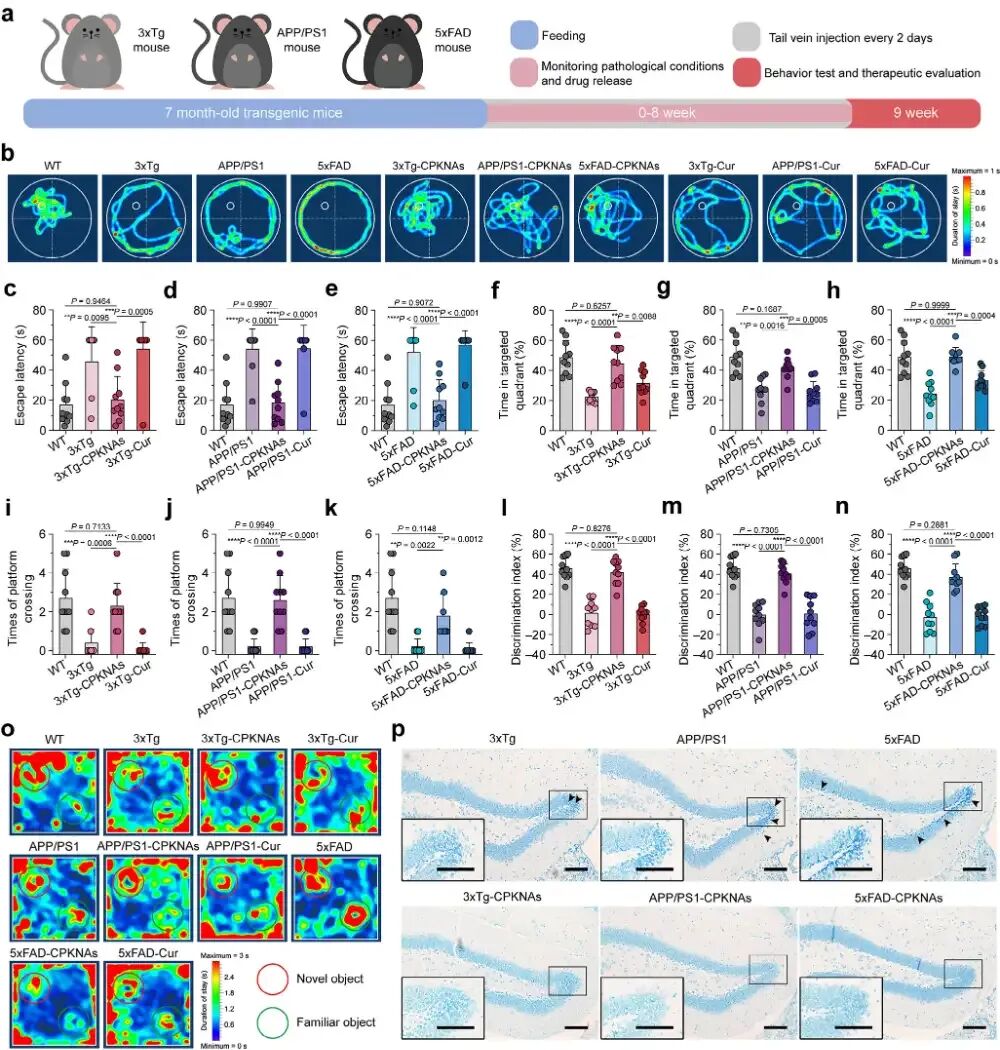
图3. CPKNAs在三种不同AD阶段转基因小鼠中的治疗效果: (a) 给药方案和行为测试示意图:8周治疗,每两天静脉注射一次,Cur当量20 mg/kg。(b) MWM测试中代表性热图。(c-k) 逃避潜伏期、目标象限停留时间百分比和平台穿越次数的定量分析:CPKNAs显著优于游离Cur,在三种小鼠中均达到接近WT对照的水平。(l-o) NOR测试及辨别指数(DI):CPKNAs处理的转基因小鼠辨别指数与WT对照相当。(p) 海马组织Nissl染色:CPKNAs处理组与WT对照无明显形态学差异,游离Cur处理组显示不同程度的神经元萎缩(黑色箭头)。
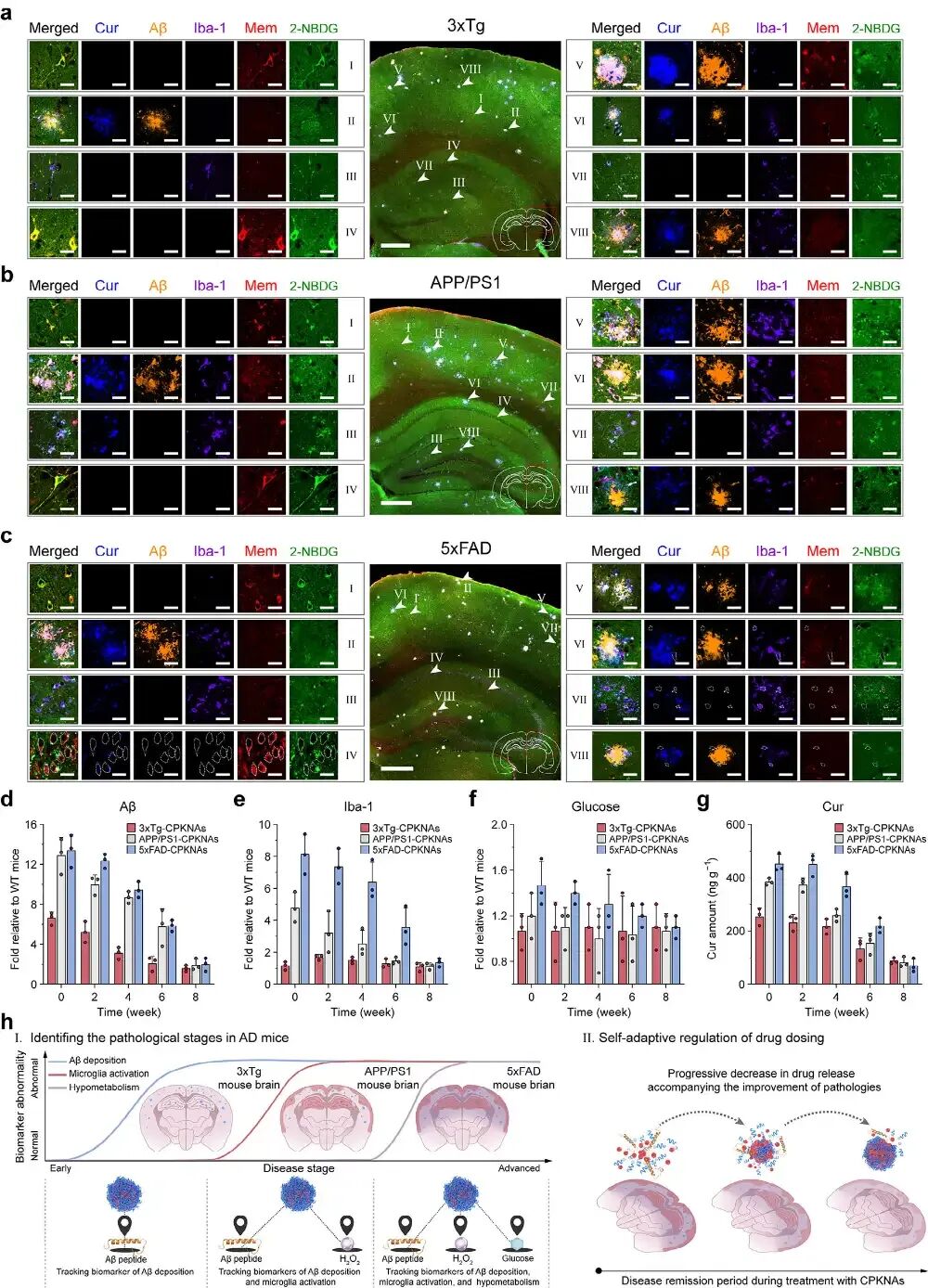
图4. CPKNAs在AD转基因小鼠中跟踪病理时空坐标: (a-c) 首次静脉注射后4 h脑切片荧光成像,显示释放的Cur(蓝色)与Aβ斑块(橙色)共定位(a,3xTg)、与Aβ斑块和活化小胶质细胞(紫色)共定位(b,APP/PS1)、以及与Aβ斑块、活化小胶质细胞和糖代谢障碍区域(2-NBDG绿色滞留减少)共定位(c,5xFAD)。(d-g) 治疗过程中脑内释放Cur水平与Aβ₄₀(d)、Iba-1(e)、葡萄糖(f)水平的动态变化,以及三者与释放Cur的相关性(g):随着治疗进行,生物标志物水平下降,释放Cur同步减少,呈动态适应。(h) CPKNAs动态追踪病理分期并自适应调节脑内药物分布的机制示意图。
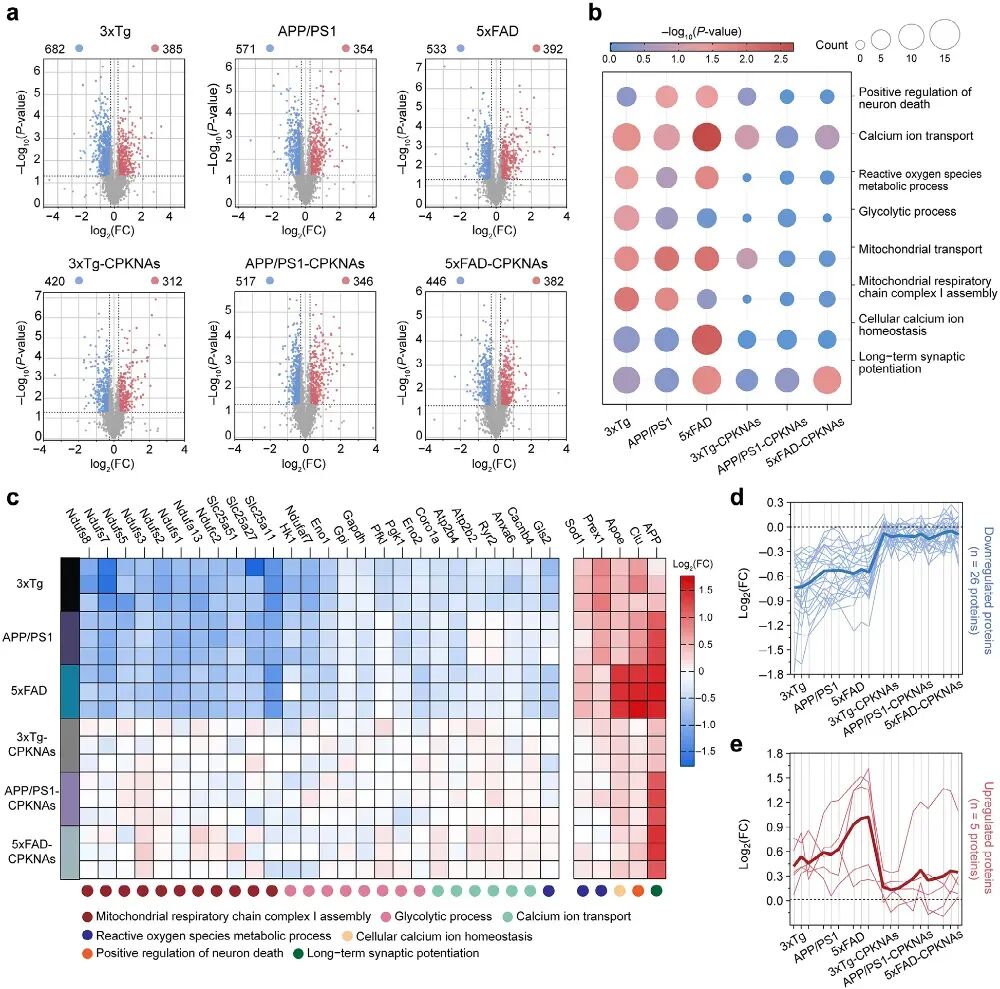
图5. CPKNAs处理AD小鼠大脑的蛋白质组学分析: (a) WT与未处理或CPKNAs处理转基因小鼠之间的DEPs火山图:CPKNAs处理后,与WT之间的DEPs数量显著减少。(b) GO富集分析点图:CPKNAs处理后,AD相关生物学过程富集的蛋白数量和显著性均降低。(c) 热图展示代表性DEPs在未处理转基因小鼠大脑中的上调或下调,以及CPKNAs处理后的相应变化,涉及Ca²⁺稳态失衡、氧化应激/神经炎症和能量代谢障碍等生物学过程。(d-e) 下调蛋白(d)和上调蛋白(e)丰度分布图,蓝/红线表示各蛋白表达变化,深蓝/红线为均值趋势。
结论
本研究开发了一种基于动态共价苯硼酸酯键的层次响应性肽-药物偶联物CPKNAs。该纳米药物能够解码Aβ、ROS和葡萄糖三个关键AD进展生物标志物的时空演变模式,根据病变严重程度自适应性调节药物释放剂量和脑内分布。在七种细胞模型和三种不同AD阶段的转基因小鼠中,CPKNAs在统一给药方案下实现了持续一致的治疗效果,有效减轻了细胞损伤、改善了记忆和认知缺陷,同时避免了传统游离姜黄素的双相剂量-反应问题和误用药风险。该策略为应对AD进展的异质性提供了新的治疗范式,通过“同药、同剂量、自适应”的方式,有望简化临床试验设计、提高患者依从性,并扩大药物治疗在异质性AD人群中的适用范围。
原文链接:
https://doi.org/10.1002/adma.202516343


