中科院上海营养与健康所,最新Science大子刊:急性髓系白血病的新型治疗靶点
时间:2026-05-09 21:32:24 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
急性髓系白血病复发率高、预后差,耐药白血病干细胞是复发主因,临床亟需安全有效的新靶点。RNA结合蛋白RBPMS在AML中高表达且受关键致癌融合蛋白调控,但在白血病中的功能与机制尚不明确,同时肿瘤糖代谢重编程对白血病进展至关重要,而RNA结合蛋白调控白血病代谢的机制仍待解析。
中国科学院大学上海营养与健康所王兰研究员,上海交通大学孙晓建研究员等人系统揭示了RBPMS在急性髓系白血病中的关键作用与调控机制,并成功研发出靶向该蛋白的特异性小分子抑制剂。相关内容以“Targeting RBPMS selectively eliminates FOXO1-mediated stem cell signatures in mouse models of acute myeloid leukemia”为题发表在《Science Translational Medicine》上。

【主要内容】
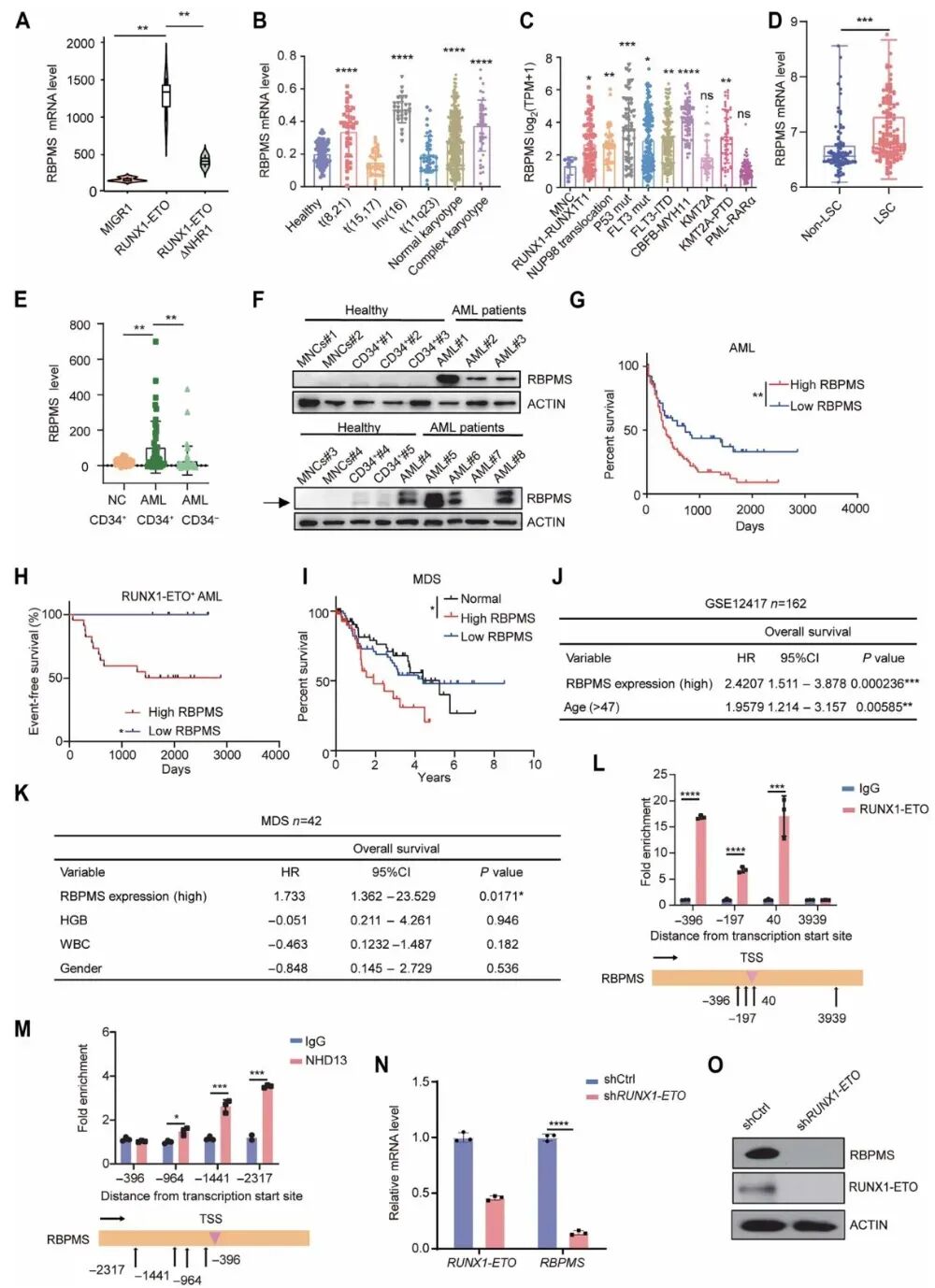
图1 RBPMS在急性髓系白血病中高表达并与不良预后相关
数据显示AML患者体内RBPMS水平显著高于健康人群,在RUNX1‑ETO、NUP98易位等特定亚型中表达更高,且高表达RBPMS的AML及骨髓增生异常综合征患者总生存期更短,同时证实RUNX1‑ETO与NUP98‑HOXD13可直接结合RBPMS启动子并激活其转录。
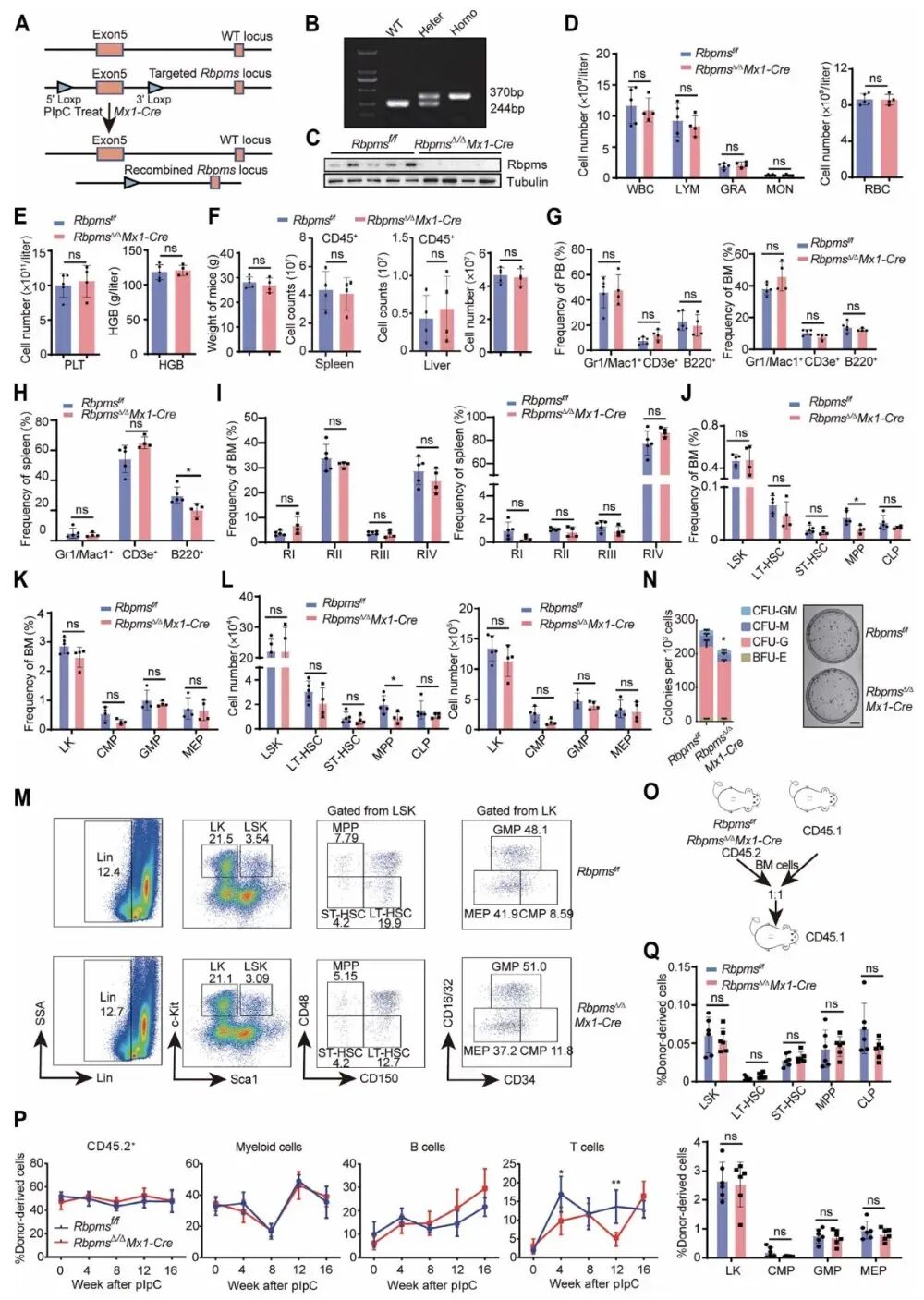
图2 评估RBPMS对正常造血系统的影响
上图显示敲除Rbpms后小鼠外周血细胞计数、各系成熟血细胞比例、造血干祖细胞数量与分化能力均未出现明显异常,骨髓竞争性移植实验也证实Rbpms缺失不影响正常造血干细胞的重建功能。
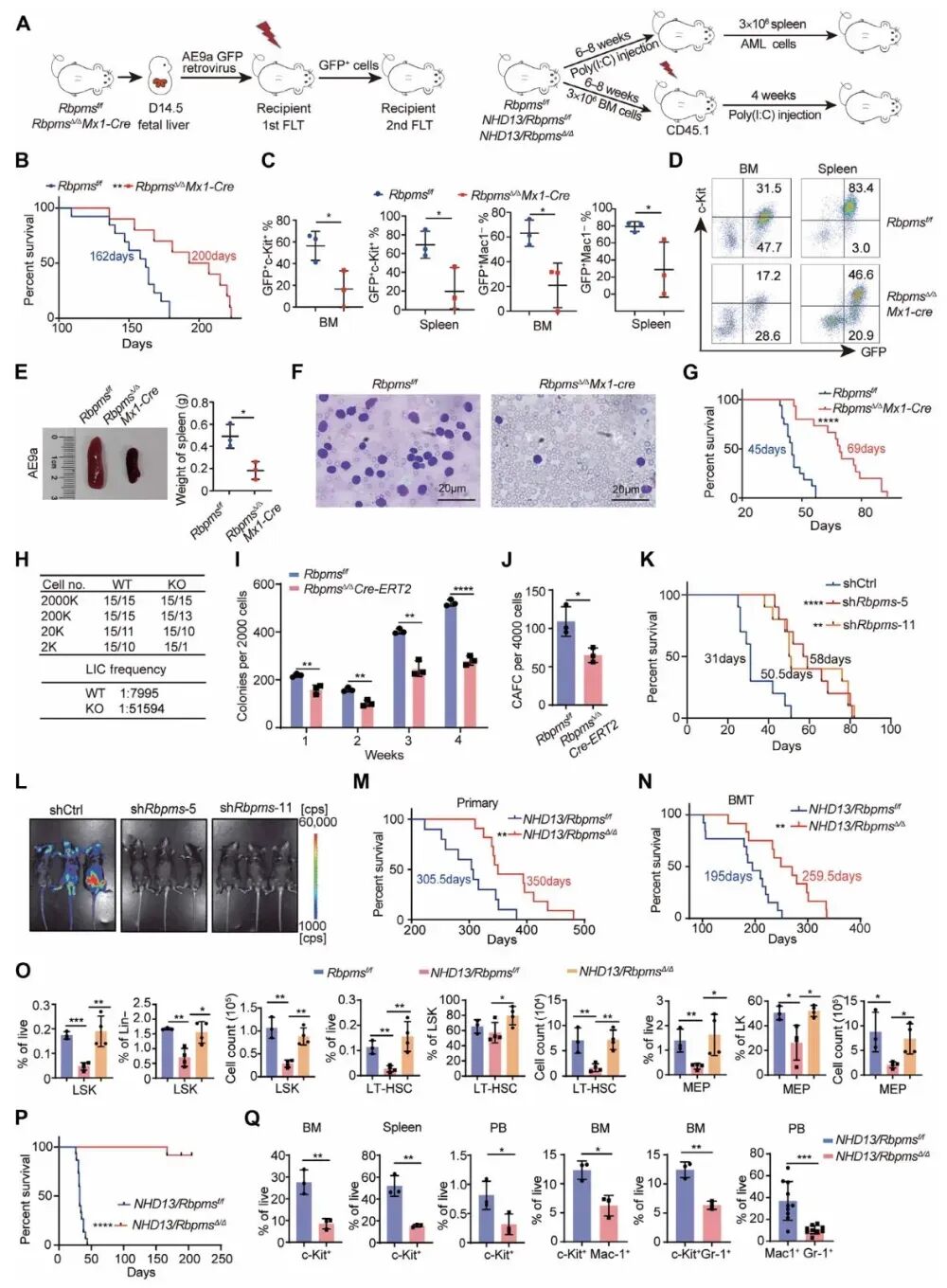
图3 RBPMS缺失可显著延缓白血病进展
在RUNX1‑ETO9a与NUP98‑HOXD13驱动的AML模型中,Rbpms敲除降低体内白血病负荷、减少脏器浸润并延长小鼠生存期,同时降低白血病起始细胞频率、抑制其自我更新能力。
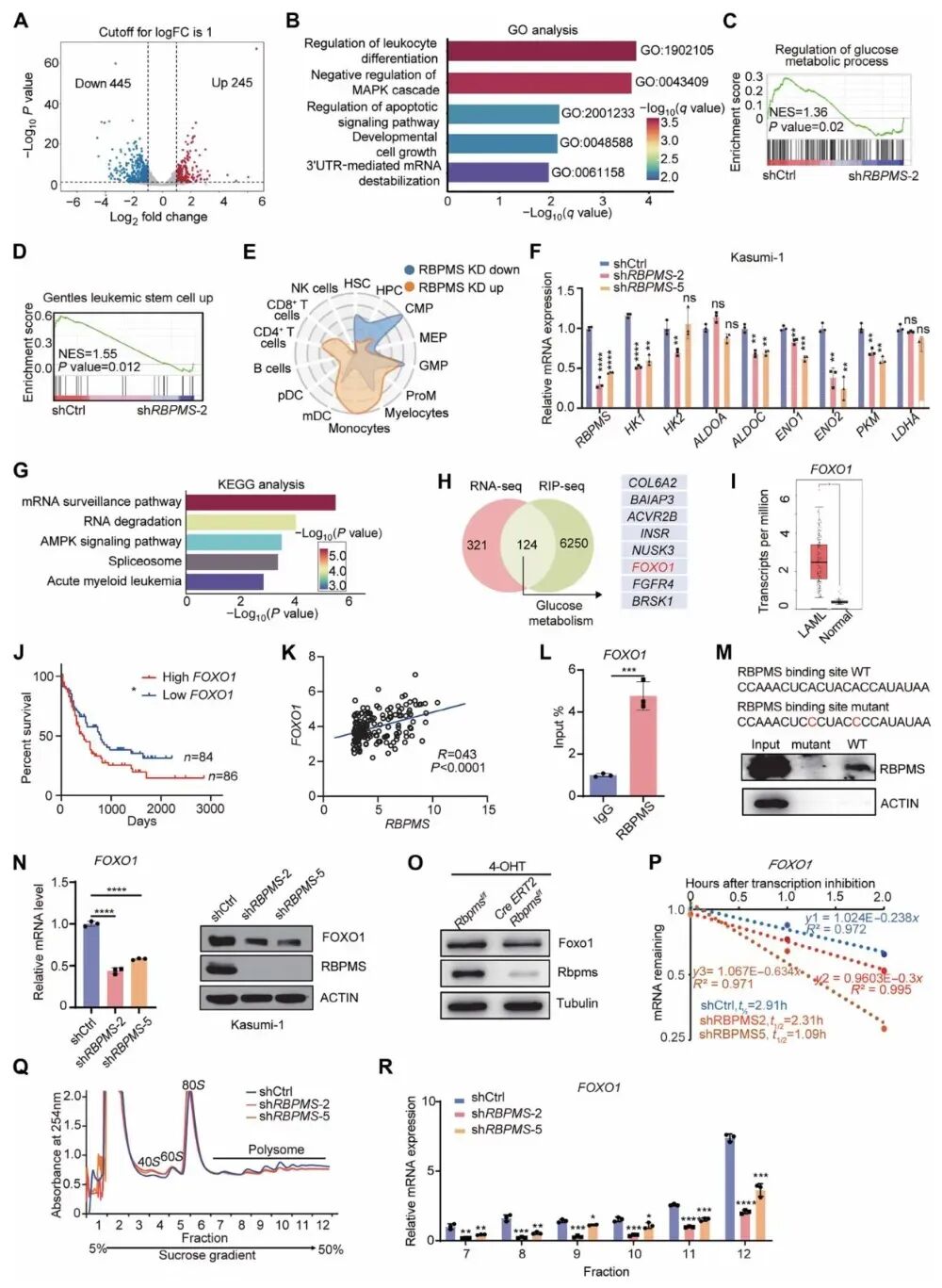
图4 FOXO1是RBPMS的直接下游靶基因
上图证实RBPMS可直接结合FOXO1 mRNA并增强其稳定性与翻译效率,RBPMS敲低会显著下调FOXO1表达,且二者在AML患者中呈显著正相关,同时发现RBPMS通过FOXO1调控白血病细胞的糖代谢相关基因表达。
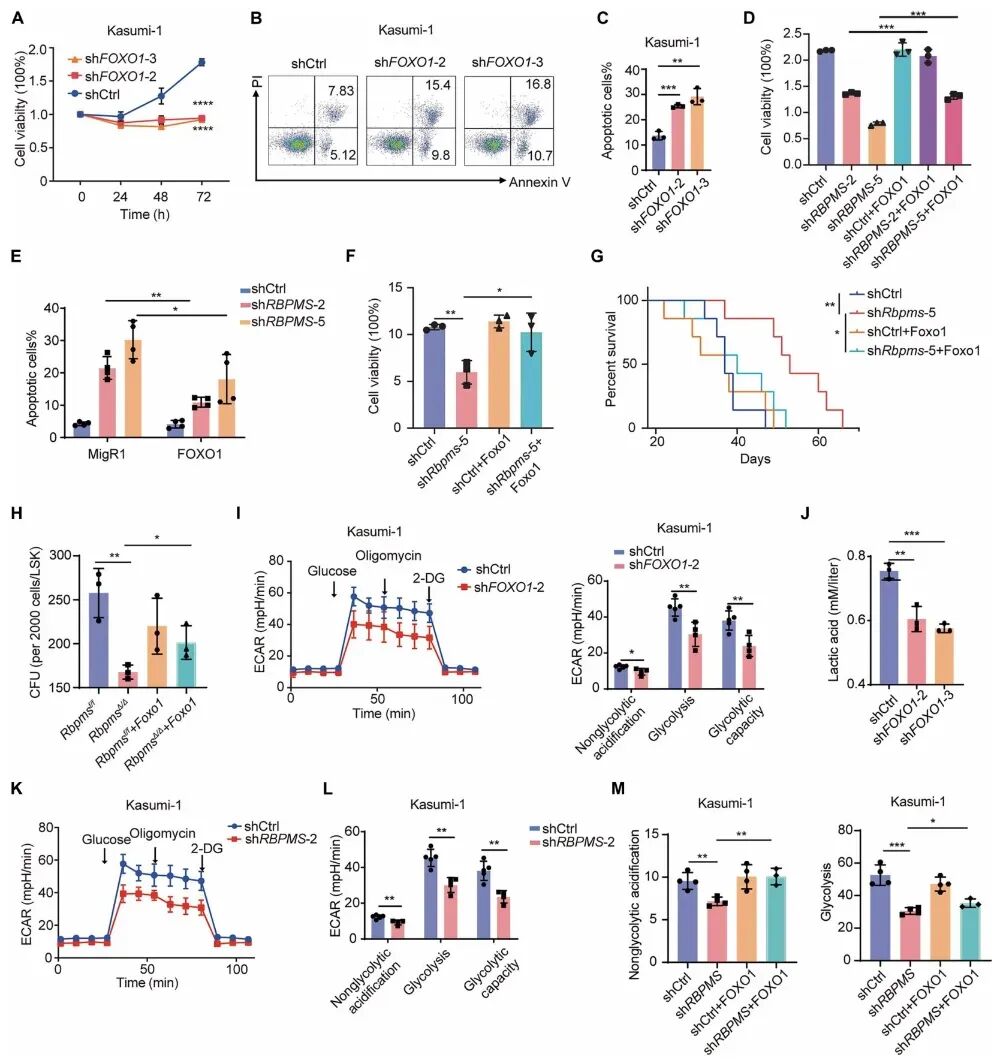
图5 FOXO1是RBPMS调控白血病的关键效应分子
敲低FOXO1可模拟RBPMS缺失的表型,抑制白血病细胞增殖、诱导凋亡并降低糖酵解水平,而过表达FOXO1能够逆转RBPMS敲低导致的细胞生长抑制、干性下降与代谢异常。
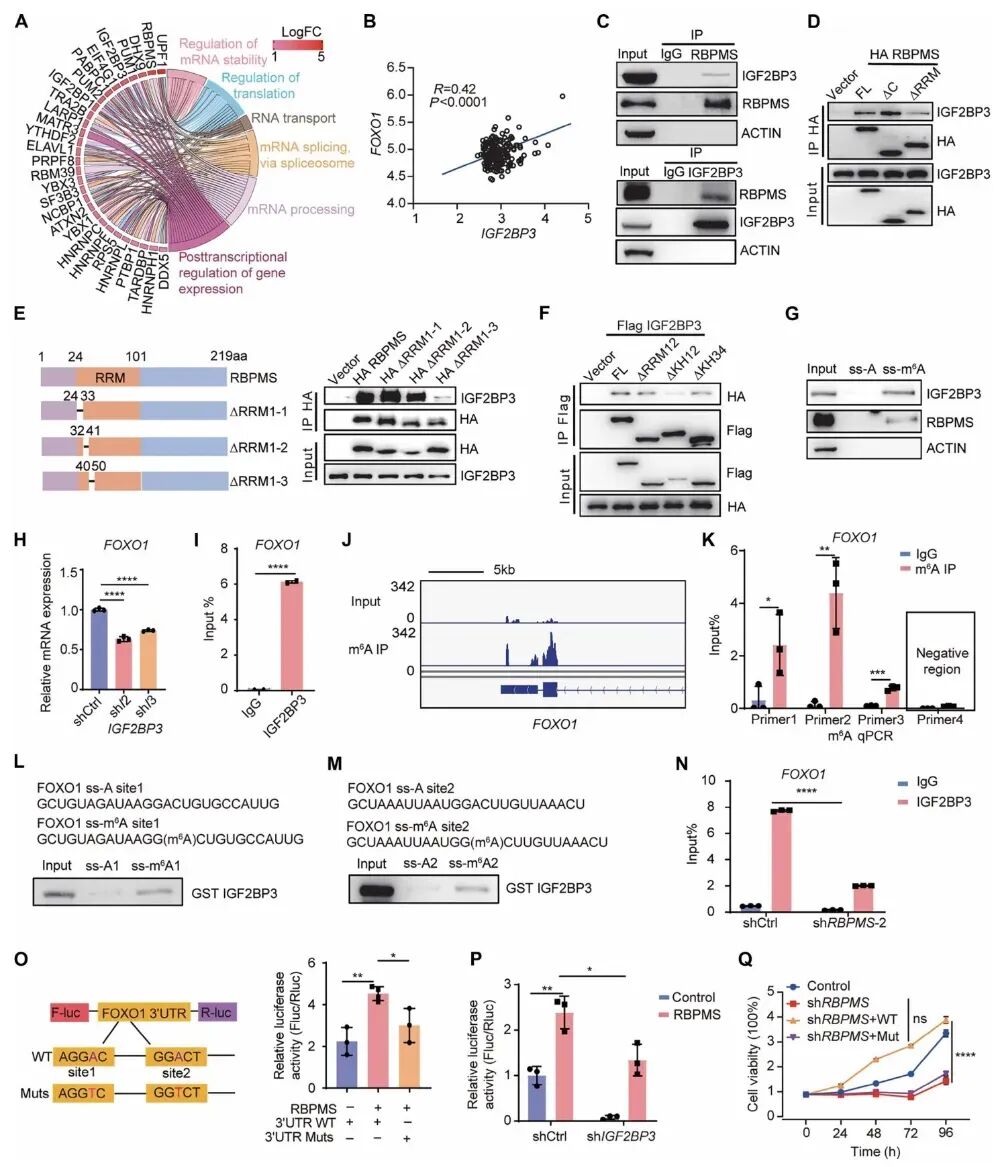
图6 RBPMS调控FOXO1的分子机制
上图证实RBPMS与m⁶A阅读蛋白IGF2BP3直接相互作用,二者以m⁶A修饰依赖的方式共同稳定FOXO1 mRNA,IGF2BP3是RBPMS上调FOXO1的必需分子,破坏二者结合或敲低IGF2BP3都会阻断FOXO1表达并抑制白血病细胞恶性表型。
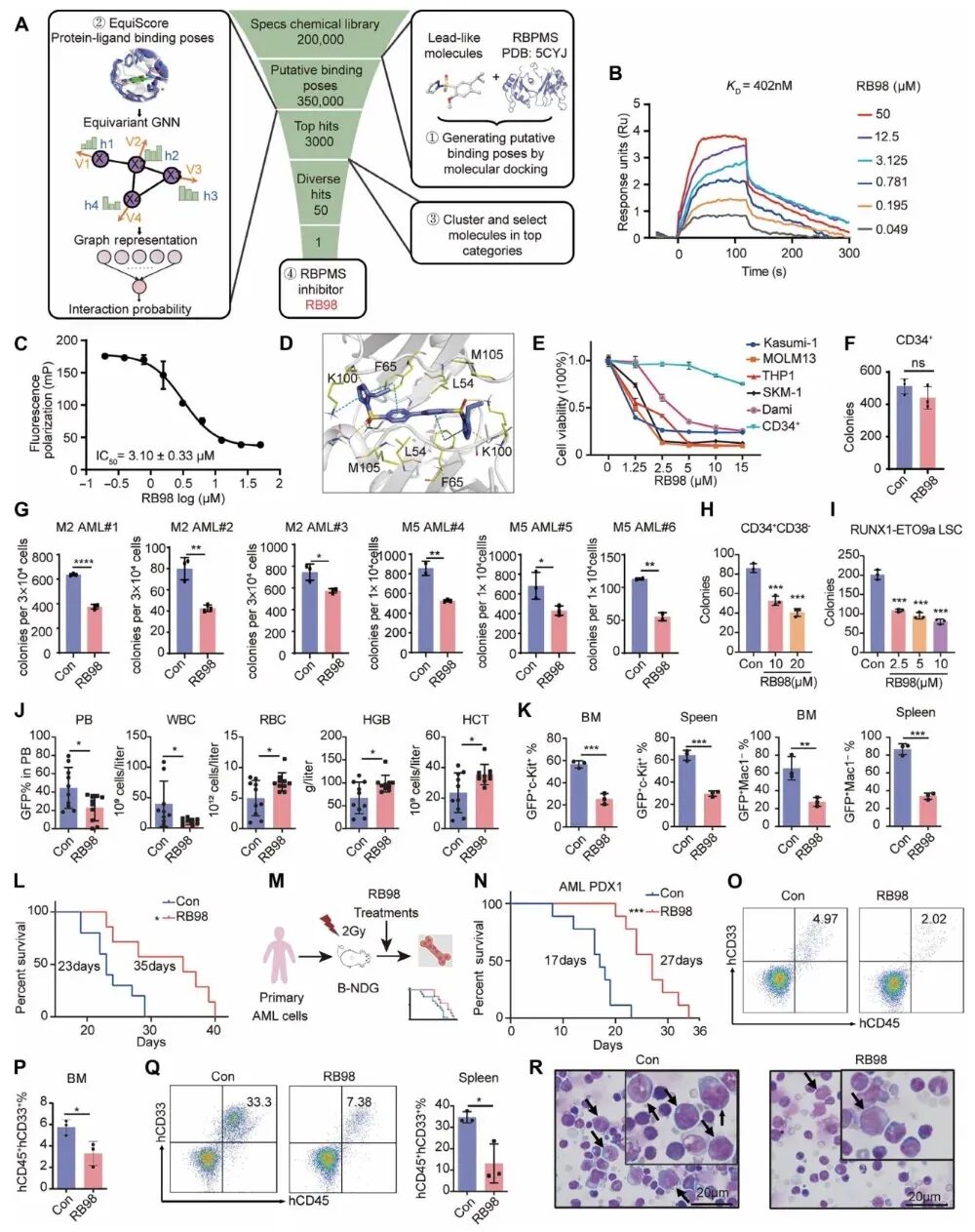
图7 靶向RBPMS的小分子抑制剂RB98的筛选、验证与治疗效果
RB98可特异性结合RBPMS的RRM结构域,阻断其与FOXO1 mRNA结合,在体外显著抑制AML细胞增殖与干性、降低糖酵解,在小鼠AML模型与患者来源异种移植模型中有效降低白血病负荷、延长生存期,且对正常造血与肝肾功能无明显毒性。
【全文总结】
本研究完整揭示了RBPMS‑IGF2BP3‑FOXO1调控轴在AML中的核心作用,并成功研发首个靶向RBPMS的候选药物,为急性髓系白血病提供了全新的治疗策略与转化方向。
原文链接:
https://doi.org/10.1126/scitranslmed.adv8951


