RNA-NGS测序助力唾液腺肿瘤精准诊断,25%的患者临床管理预期改变
时间:2026-05-09 21:25:27 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
本研究评估一款综合性 RNA 测序检测 panel(“SalvGlandDx 第 2 版”)在唾液腺肿瘤诊疗流程中的诊断检出率与临床影响。2021 年至 2025 年间,对 118 例唾液腺肿瘤先进行常规组织学与 IHC 检查,随后行 SalvGlandDx v2 RNA 测序。该 panel 靶向唾液腺肿瘤中反复出现的分子变异。对比测序前与测序后的(鉴别)诊断,以确定其诊断贡献,分为诊断确认(1A)、诊断细化(1B/2A/2B)或无影响(3)。对比测序前与测序后的(鉴别)诊断,将临床影响评为无影响(A)、随访方案改变(B)、放疗指征改变(C)和 / 或全身治疗改变(D)。
118 例中 114 例 RNA 测序获得成功(97%)。114 例中有 78 例检出分子变异(68%),最常见的包括多形性腺瘤(癌在多形性腺瘤中,即多形性腺瘤恶变)的 PLAG1 与 HMGA2 重排、黏液表皮样癌的 MAML2 重排。114 例中有 66 例实现了诊断细化(58%),其中 29 例(25%)测序前诊断得到确认,37 例(32%)测序前鉴别诊断得到细化。114 例患者中有 29 例的临床管理受到影响(25%),最常影响的是随访频次。
综合性 SalvGlandDx v2 RNA 测序在唾液腺肿瘤中表现出较高的可行性,以及显著的诊断与临床应用价值,能够解决形态学与 IHC 难以明确的病例。在一部分患者中,该检测的应用还会影响临床管理,凸显将 RNA 测序整合进种类繁多、诊断具有挑战性的唾液腺肿瘤常规诊疗流程中的价值。
-
综合性 RNA 测序可优化唾液腺肿瘤的分类。
-
58% 的受检病例实现了诊断细化。
-
RNA 测序有助于形态不典型唾液腺肿瘤的诊断。
-
RNA 测序结果对 25% 的病例产生临床管理影响。
研究背景
近年来,随着对基因组图谱认知的不断加深,唾液腺肿瘤的分类发生了相当大的变化。近期新增的基因组变异包括,例如所谓 “导管内” 癌中的 RET 重排,以及纹状管腺瘤中的 IDH2 突变。第 5 版 WHO 头颈部肿瘤分类目前收录了近 40 种独立亚型,其中许多都具有特征性基因组变异。因此,分子谱分析不仅能够辅助唾液腺肿瘤的(重新)分类,还能提高形态学不典型病变的诊断准确性。
分子分析可通过多种方式开展,常包括 FISH 和 / 或基于 DNA/RNA 测序的检测。在部分亚型中,IHC 标志物可作为其潜在分子变异的替代指标,例如腺泡细胞癌中细胞核 NOR1(NR4A3)的 IHC 表达。然而,对于唾液腺肿瘤标本量较少的病理科而言,全面开展各类 IHC 与分子检测往往难以实现。因此,诊断上具有挑战性的病例常被送往外院会诊以完成最终分型。本院在唾液腺肿瘤的诊疗流程中已应用多种分子技术,包括 DNA 与 RNA 测序分析。由于融合驱动型唾液腺肿瘤数量可观,RNA 测序的价值尤为突出。为此,一款专为唾液腺肿瘤设计的综合性 RNA 测序 panel 被引入本院常规诊断工作。最新研发的 SalvGlandDx v2 panel 纳入了多数具有诊断与临床意义的基因重排、热点突变,以及特定基因的 RNA 表达分析,可高效检出临床常见的分子变异。SalvGlandDx panel 此前已在细针穿刺标本中辅助唾液腺肿瘤的分型。
本研究旨在评估综合性 RNA 测序 panel 在唾液腺肿瘤诊断中的诊断检出率。其次,本研究旨在展示 RNA 测序在临床实践中对临床管理的影响。研究者假设,在唾液腺切除标本中实施 SalvGlandDx v2 RNA 测序可提供显著的诊断细化,并进而影响后续临床管理决策。
研究方法
2021 年 1 月至 2025 年 1 月,共有 139 例原发性唾液腺肿瘤的 FFPE 标本采用定制 RNA 测序 SalvGlandDx v2 panel(ArcherDx,美国博尔德市)进行测序,该 panel 已纳入莱顿大学医学中心的常规诊断。该综合性 panel 覆盖唾液腺肿瘤中已知的分子变异。
分子分析对最终诊断的影响分类如下:
-
SalvGlandDx v2 RNA 分析得出明确亚型,可确认单一诊断(1A),或将鉴别诊断缩小为单一亚型(1B)。
-
SalvGlandDx v2 RNA 分析区分良恶性,但未明确单一亚型,得出仅含良性病变的鉴别诊断(2A),或仅含恶性病变的鉴别诊断(2B)。
-
SalvGlandDx v2 RNA 分析未改变鉴别诊断(3)。
该评分体系可反映分子分析对(鉴别)诊断的价值,其中 1B、2A、2B 类别具有诊断价值,1A 与 3 类别无诊断价值。表 1 列出了用于评估分子分析诊断价值的分类。本队列中有少数病变被归类为伴非典型特征的多形性腺瘤(PA),这凸显出一组在区分原位 / 包膜内癌在多形性腺瘤中(CXPA)与 PA 时仍存在困难的病变,尤其当出现显著细胞核异型、轻中度核分裂活性、包膜侵犯和 / 或广泛间质玻璃样变时。若未观察到明显细胞核异型、双层导管与肌上皮结构保留,且无其他高危分子特征(如 TP53 突变和 / 或 HER2 扩增),则诊断为伴非典型特征的 PA。
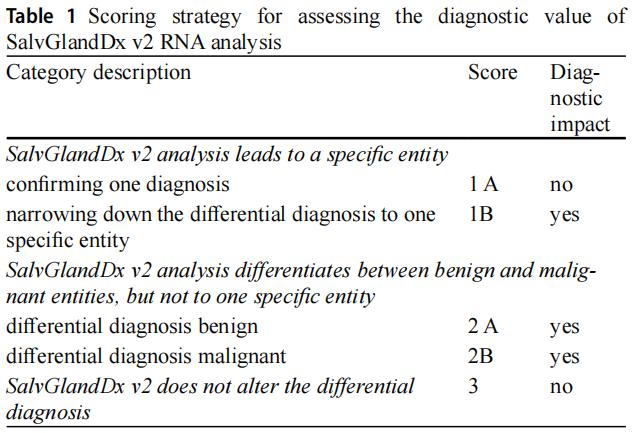
表1
为评估分子分析对治疗选择的影响,采用既定评分体系。由资深头颈部外科医师(SvE)对每一例病例判定,测序前与测序后的(鉴别)诊断是否符合以下一项或多项分类:无临床影响(A)、随访频次改变(B)、放疗指征改变(C)、全身治疗改变(D)。
研究结果
研究队列:
最终 118 例队列包括原发性唾液腺肿瘤切除标本(n=93)与活检标本(n=26)。肿瘤部位不一,75 例肿瘤(64%)位于大唾液腺(腮腺、下颌下腺),42 例肿瘤(36%)位于小唾液腺。118 例中 114 例 RNA 测序成功(97%),3 例因陈旧标本(切除时间 > 10 年)RNA 质量不足导致测序失败,1 例为骨化后脱钙的多形性腺瘤测序失败。SalvGlandDx v2 panel 在 114 例中的 78 例(68%)检出分子变异(重排、突变或 RNA 过表达)。经 H&E、IHC 与分子分析后,97 例(85%)获得最终诊断。其中包括 41 例良性肿瘤:多形性腺瘤(n=33)、基底细胞腺瘤(n=3)、嗜酸细胞瘤(n=2)、沃辛瘤(n=1)、唾液腺囊腺瘤(n=1)、纹状管腺瘤(n=1)。56 例恶性肿瘤包括:癌在多形性腺瘤中(n=11)、黏液表皮样癌(n=13)、腺泡细胞癌(n=7)、多形性腺癌(n=6)、腺样囊性癌(n=5)、上皮 - 肌上皮癌(n=5)、分泌性癌(n=2)、导管内癌(n=2)、透明样透明细胞癌(n=2)、肌上皮癌(n=1)、黏液腺癌(n=1)、唾液腺癌非特指型(n=1)。癌在多形性腺瘤中的组织学恶性成分包括:唾液腺导管癌(n=3)、肌上皮癌(n=6)、唾液腺癌非特指型(n=2)。17 例在测序成功后仍为鉴别诊断。
检出分子变异谱:
检出重排:
62 例检出重排,这些病例的汇总见图 1 。PLAG1 重排在 25 例标本中检出,融合伴侣多样:FGFR1(n=6)、CTNNB1(n=5)、NCALD(n=4)、ACTA2(n=2)、LIFR(n=2)、STAMBLI(n=1)、GEM(n=1)、UBC(n=1)、TGFBR3(n=1)、FBXO32(n=1)、LOC101928323(n=1)。其中 17 例伴 PLAG1 重排的肿瘤诊断为多形性腺瘤,包括 1 例肌上皮为主肿瘤(GEM::PLAG1)、1 例含嗜酸细胞成分肿瘤(UBC::PLAG1)、2 例伴非典型特征肿瘤(NCALD::PLAG1、LOC101928323::PLAG1)。7 例伴 PLAG1 重排的肿瘤诊断为癌在多形性腺瘤中,其中 3 例恶性成分为肌上皮癌(NCALD::PLAG1、NCALD1::PLAG1、FGFR1::PLAG1),2 例为唾液腺导管癌(CTNNB1::PLAG1、FGFR1::PLAG1),1 例为腺癌非特指型(FGFR1::PLAG1)。1 例病例归类为非典型肌上皮肿瘤,鉴别诊断为肌上皮瘤与肌上皮癌,携带 TGFBR3::PLAG1 融合。该病变呈显著多叶生长,伴广泛硬化间质背景,且切除不完全,限制了最终共识分型。TGFBR3::PLAG1 融合近期由 Rupp 等人(2021)在一组形态特征相似的病变中报道 。结合显著形态特征、切除不完全以及无额外 TP53 突变和 / 或 HER2 扩增,最终给出描述性共识诊断。
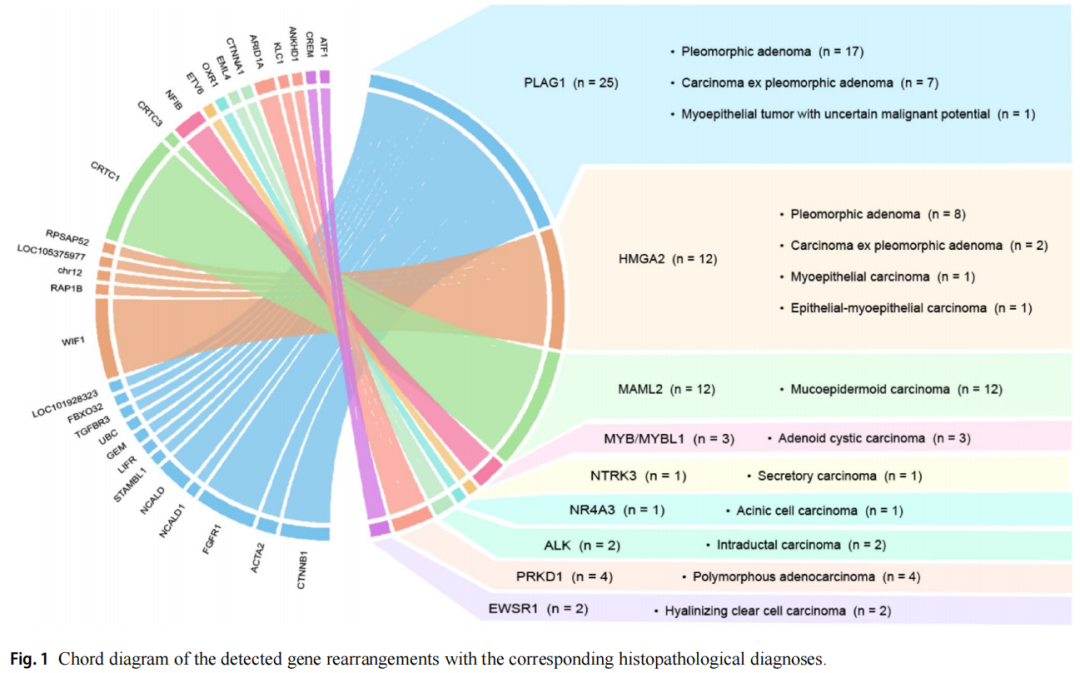
图1
HMGA2 重排在 12 例标本中检出,均涉及 HMGA2 基因 3 号外显子断裂点,融合伴侣多样:WIF1(n=8)、RAP1B(n=1)、LOC105375977(n=1)、RPSAP52(n=1)、12 号染色体基因间区(n=1)。其中 8 例伴 HMGA2 重排的肿瘤诊断为多形性腺瘤,包括 2 例呈小管样结构(HMGA2::WIF1)、1 例肌上皮为主肿瘤(HMGA2::WIF1)、1 例伴非典型特征肿瘤(HMGA2::WIF1)。3 例癌在多形性腺瘤中携带 HMGA2::WIF1 重排,其中 2 例主要恶性成分为肌上皮癌,1 例为上皮 - 肌上皮癌。值得注意的是,2 例肌上皮癌型癌在多形性腺瘤在额外 DNA NGS 分析中均显示 MDM2 与 CDK4 扩增。1 例肌上皮癌(HMGA2::chr12 基因间区)未见到经典多形性腺瘤成分。
MAML2 重排在 12 例标本中检出,与 CRTC1(n=11)或 CRTC3(n=1)配对。所有病例均诊断为低级别黏液表皮样癌。PRKD1 重排在 4 例标本中检出,与 ARID1A(n=2)、KLCI(n=1)、ANKHD1(n=1)配对。所有肿瘤均诊断为多形性腺癌。未检出多形性腺癌中常见的、多伴经典形态的 PRKD1 p.E710D 点突变。MYB 重排在 2 例标本中检出,两例融合伴侣均为 NFIB。第 3 例检出 MYBL1::NFIB 重排,DNA NGS 分析显示额外 KRAS 与 TP53 突变及 PTK2 获得。组织形态学上该病例无高级别特征,呈管状与筛状生长方式,无实性生长,肌上皮细胞 p63 IHC 表达阳性。3 例伴 MYB/MYBL1 重排的病例均诊断为腺样囊性癌。EWSR1 重排在 2 例标本中检出,融合伴侣为 ATF1(n=1)与 CREM(n=1)。两例最终切除标本均诊断为透明样透明细胞癌。1 例透明样透明细胞癌见图 2。
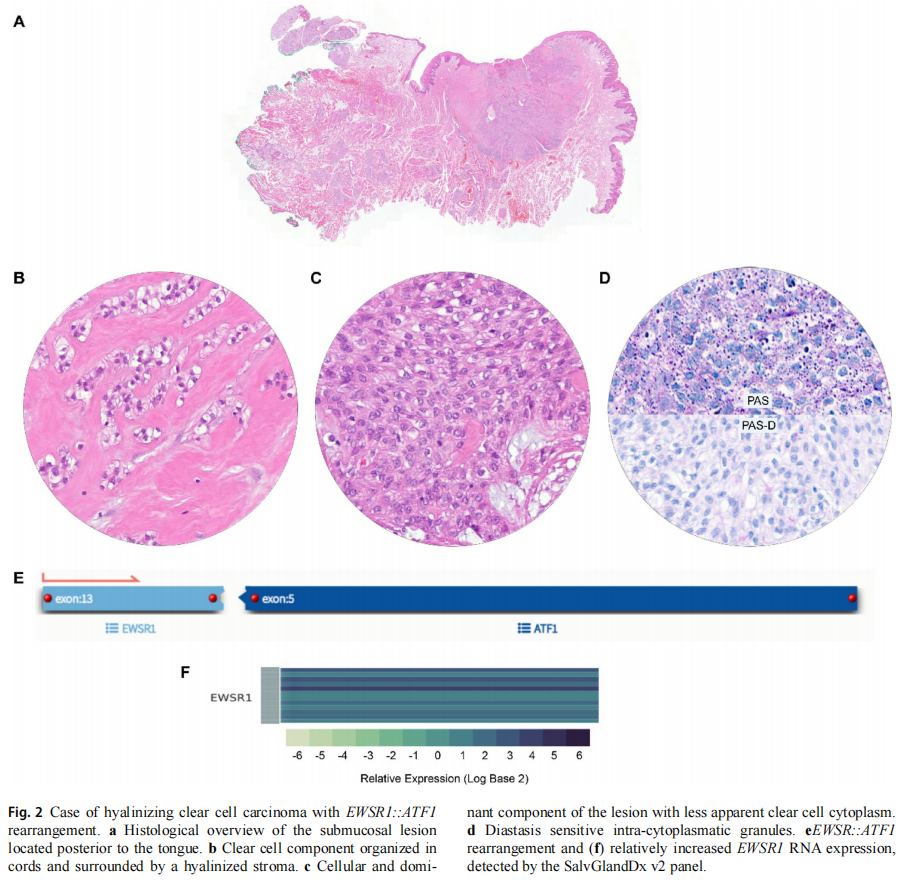
图2
酪氨酸激酶重排在 3 例中检出,涉及 ALK 与 NTRK。ALK 重排在 2 例标本中检出,融合伴侣为 EML4(n=1)与 CTNNA1(n=1)。两例最终切除标本均诊断为导管内癌,1 例见图 3。
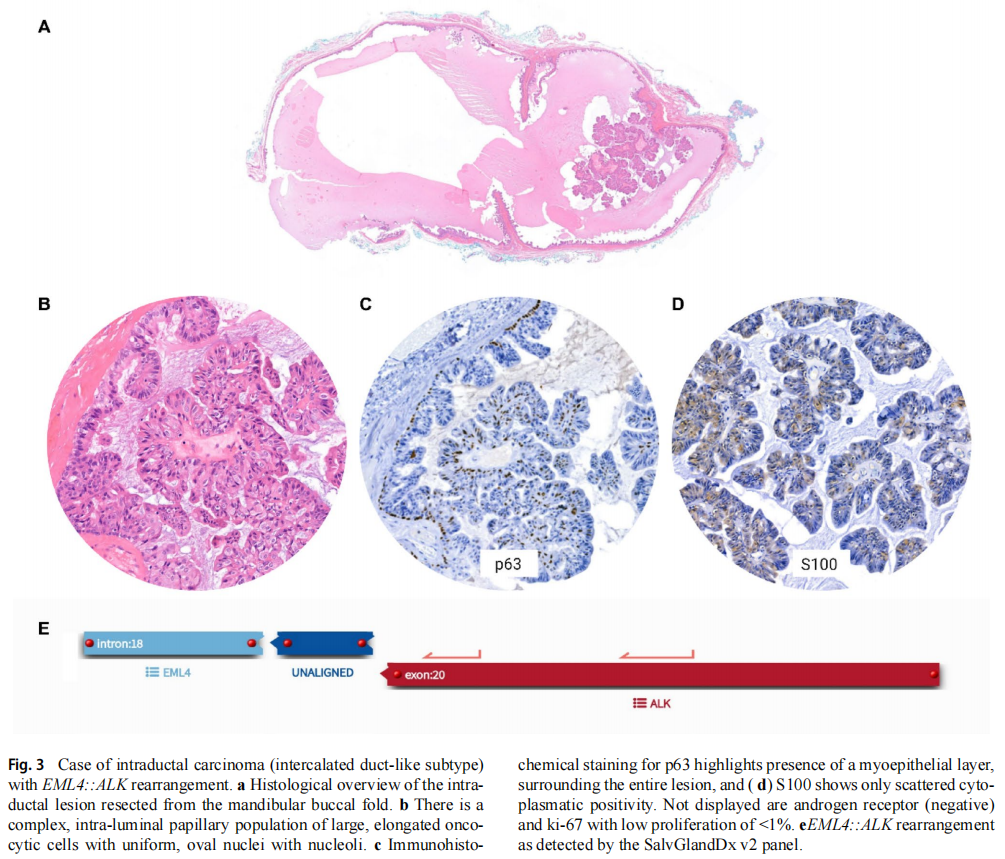
图3
NTRK3 重排在 1 例标本中检出,与 ETV6 配对。该病变诊断为分泌性癌。1 例检出 OXR1::NR4A3 重排,最终切除标本诊断为腺泡细胞癌(嗜酸细胞亚型)。该重排通过启动子置换导致 NR4A3 转录上调。第 2 例腺泡细胞癌同样显示 NR4A3::4 号染色体基因间区重排。该病例见图 4。
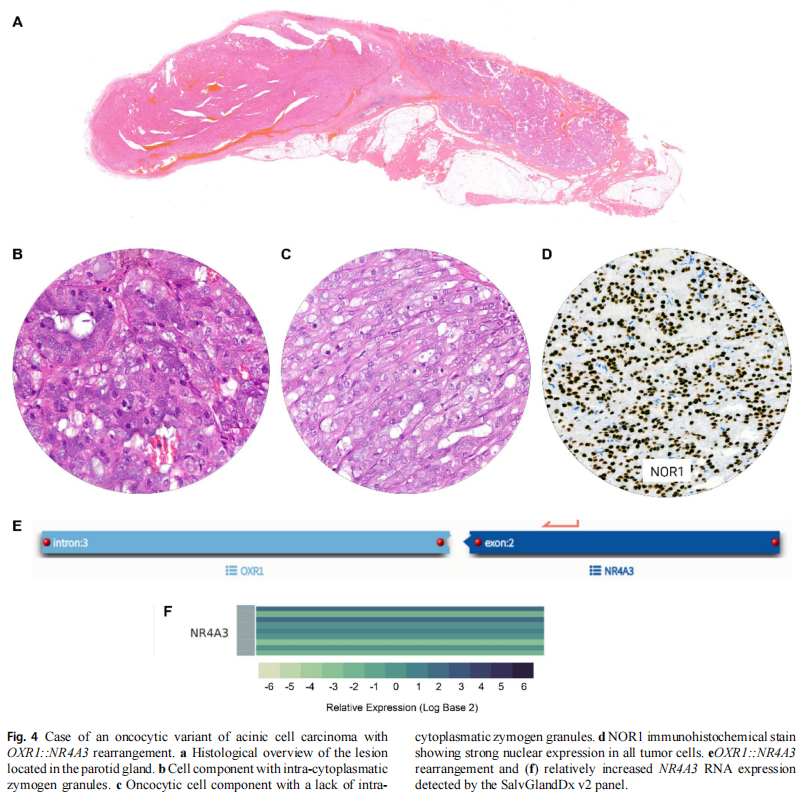
图4
检出突变:
16 例检出单核苷酸变异 / 体细胞突变。HRAS 突变在 5 例恶性肿瘤中发现,包括 4 例上皮 - 肌上皮癌。1 例伴 HRAS 突变的肿瘤显示 p63、p40、CK5/6、CK7 弥漫 IHC 阳性,雄激素受体、HER2、钙调蛋白、S100、SOX10 IHC 染色阴性。该病例归类为高级别单相癌,无明确肌上皮成分,最符合转移性鳞状细胞癌。CTNNB1 突变在 4 例中检出,均归类为基底细胞腺瘤。2 例基底细胞腺瘤 β- 连环蛋白 IHC 染色显示局灶弱核阳性,回顾符合阳性结果。AKT1 突变见于 2 例肿瘤,1 例为伴发 HRAS 突变的上皮 - 肌上皮癌,1 例为黏液腺癌。PIK3CA 突变在 2 例肿瘤中检出,1 例为伴 CTNNB1::PLAG1 重排的唾液腺导管癌型癌在多形性腺瘤中,1 例为 NFIB RNA 高表达的恶性肿瘤。后者肿瘤鉴别诊断广泛,首先考虑腺样囊性癌、基底细胞腺癌、唾液腺癌非特指型。
RNA 表达升高:
3 例最终切除诊断为腺泡细胞癌的病例检出 NR4A3 RNA 过表达(图 4),其中 1 例未检出重排。2 例检出 HMGA2 过表达,其中 1 例伴 HMGA2::WIF1 重排。1 例在无重排情况下显示 MYB RNA 相对升高。该肿瘤诊断为腺样囊性癌。由于 HMGA2 与 MYB 表达分析仍在验证中,这些结果视为探索性。
诊断影响:
为评估 SalvGlandDx v2 RNA 测序的诊断影响,所有 118 例按照表 1 所列评分体系进行评分。评分时将基于 H&E 与 IHC 的测序前(鉴别)诊断与整合 RNA 测序后的最终(鉴别)诊断进行对比。60/118 例(51%)经 RNA 测序获得明确分型:29/118 例(25%)确认疑似诊断(评分 1A),31/118 例(27%)将测序前鉴别诊断细化为单一亚型(评分 1B)。这些病例检出特征性分子重排或突变,例如伴 MAML2 重排的黏液表皮样癌、伴 PLAG1 或 HMGA2 重排的多形性腺瘤、伴 CTNNB1 突变的基底细胞腺瘤、伴 MYB 重排的腺样囊性癌。1 例疑似癌在多形性腺瘤经检出 HMGA2 重排与额外 PIK3CA 突变后得到确认。尽管评分为 1A 的病例诊断方向未改变,但对疑似诊断的确认可增强诊断信心。6/118 例(5%)经 RNA 测序将鉴别诊断细化为仅含恶性病变,未明确具体亚型(评分 2B)。其中包括 2 例测序前鉴别诊断同时含良恶性病变的病例,最终基于临床病程(1 例伴肺转移)、细胞显著细胞核异型伴强 AR IHC 表达,以及两例均检出 TP53 突变,归类为癌在多形性腺瘤中。基于 RNA 分析倾向恶性鉴别诊断会影响临床管理方向。无病例在整合 RNA 测序结果后倾向完全良性鉴别诊断(评分 2A)。剩余 48/118 例(41%)经 RNA 测序未改变或缩小鉴别诊断(评分 3)。这些病例未检出特异性重排、突变或 RNA 过表达,或检测失败。病例包括例如唾液腺癌非特指型,以及测序前鉴别诊断含恶性病变的良性病变(如嗜酸细胞瘤与腺泡细胞癌嗜酸细胞亚型、沃辛瘤与黏液表皮样癌嗜酸细胞亚型)。
118 例中共有 10 例肿瘤呈现组织形态学嗜酸细胞特征。这些肿瘤涵盖良性病变(嗜酸细胞瘤、沃辛瘤、多形性腺瘤嗜酸细胞亚型)与恶性肿瘤嗜酸细胞亚型(黏液表皮样癌、腺泡细胞癌、导管内癌、分泌性癌)。RNA 测序在 6 例嗜酸细胞病例中未检出分子变异,其中 5 例最终归类为良性,对应本队列嗜酸细胞肿瘤中阴性预测值(NPV)为 83%。相反,剩余 4 例嗜酸细胞肿瘤检出分子变异,均证实为恶性,对应阳性预测值(PPV)为 100%。若干病例经会诊中心对 H&E 与 IHC 复阅后,测序前鉴别诊断进一步缩小。这些病例同样评为 3,RNA 测序无诊断意义。RNA 测序后诊断评分与影响的病例可视化汇总见图 5。
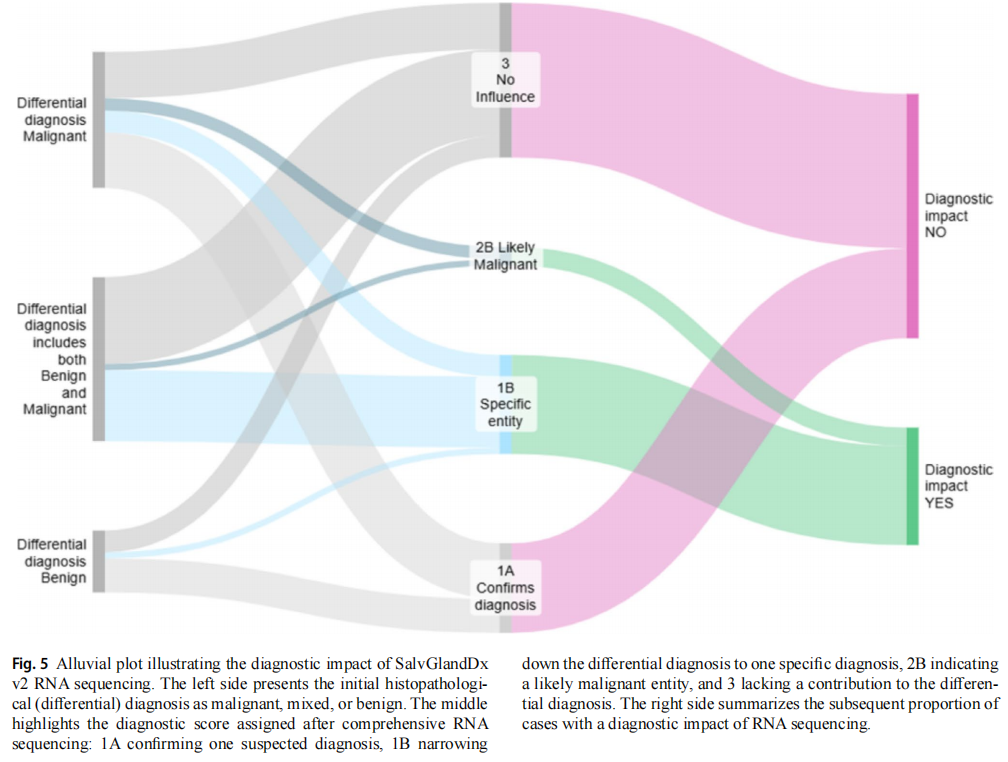
图5
临床影响:
为评估 SavlGlandDx v2 的临床意义,采用表 2 所列临床影响评分体系对鉴别诊断细化病例(评分 1B、2A、2B)进行评估。这些临床评分基于对比测序前与测序后(鉴别)诊断时临床管理的预期改变,反映诊断改变转化为临床改变的比例。部分病例预期临床管理出现多项改变,此类病例赋予多项评分。37/114 例(31%)经 RNA 测序实现鉴别诊断细化,其中 29/114 例(25%)预期临床管理发生改变(评分 B、C 和 / 或 D)。37 例有诊断影响的病例中,最常见的预期改变为随访频次(评分 B),共 26 例(70%),其次为放疗指征改变(评分 C),共 20 例(54%)。这些病例通常测序前鉴别诊断同时含良恶性病变,未给出倾向性诊断。无病例出现全身治疗改变。8/37 例(22%)预期临床管理无改变(评分 A),因这些病变已通过保守手术治疗与随访得到妥善处理。临床管理变化汇总见图 6。

表2
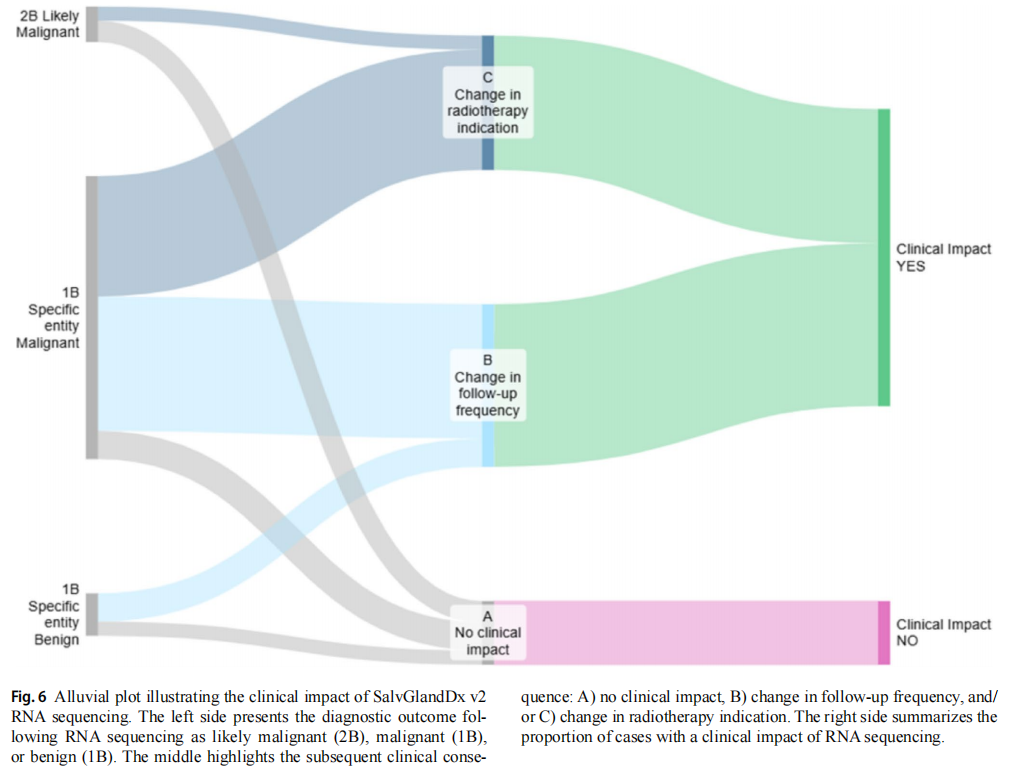
图6
讨 论
本回顾性研究在 118 例唾液腺肿瘤队列中评估了采用定制 SalvGlandDx v2 panel 进行靶向 RNA 测序的诊断与临床价值。RNA 分析可行性高,可检出广泛特征性分子变异,在 58% 的受检病例中提供诊断确认或细化(66/114 例;诊断评分 1A、1B、2B)。31% 的病例分子结果改变鉴别诊断(评分 1B/2B),额外 25% 的病例确认测序前疑似诊断(评分 1A),从而增强诊断信心。这些结果凸显将综合性 RNA 分析整合入日常诊断实践的重要性。
唾液腺肿瘤诊断中推荐采用阶梯式、保守性策略。组织形态学与靶向 IHC 分析仍是诊断基础,FISH、DNA/RNA 测序或甲基化谱分析等分子检测作为辅助手段。该阶梯式诊断策略被认为可行且高效,特征性重排(如 PLAG1、MAML2、MYB、EWSR1、RUNX2)常可通过 FISH 或替代 IHC 标志物(如腺泡细胞癌中的 NOR1)识别。然而,对于唾液腺肿瘤病例量有限的机构而言,开展广泛检测方法具有挑战性,且当融合伴侣位于同一条染色体时,FISH 可能出现假阴性结果。本研究结果显示,引入定制 RNA 测序分析可提供综合性替代方案,尤其适用于已建立分子检测、接收疑难诊断病例会诊的机构。
唾液腺肿瘤的形态多样性进一步支持开展综合性分子检测。病理医师常遇到嗜酸细胞性、基底样、透明细胞变异型,其特征跨越特定诊断亚型,同时需区分良性、中间型 / 非典型、低级别恶性病变。唾液腺肿瘤中嗜酸细胞特征的诊断挑战已由 Weinreb 等人(2009)认识。本队列中 1 例此类病例从 RNA 测序中获益,检出 UBC::PLAG1 重排,符合多形性腺瘤嗜酸细胞亚型。形态重叠或特征不典型的相似病变可对即使经验丰富的病理医师构成挑战。在鉴别诊断广泛的病变中采用综合性 RNA 测序分析可成为合理高效的诊断路径。本研究结果显示,在嗜酸细胞性唾液腺肿瘤中,RNA 测序阴性结果倾向良性肿瘤,而检出明确分子变异则对恶性具有高度预测性。
整合式综合性 RNA 测序的临床影响同样显著。25% 的病例在 RNA 测序后预期临床管理发生改变,范围从随访调整到放疗指征变更。部分仍为鉴别诊断的病例观察到临床管理方向改变,因这些病例 RNA 测序结果倾向恶性肿瘤。尽管如此,需注意临床管理还取决于手术切缘状态等因素,且不同机构临床管理可能存在差异,本研究未纳入这些因素。除诊断细化外,RNA 测序还可辅助识别可靶向的致癌驱动基因。1 例检出 NTRK 重排的病例最终确诊为分泌性癌。Le 等人(2022)报道 TRK 抑制剂拉罗替尼对携带 NTRK 重排的唾液腺肿瘤有效,支持此类恶性肿瘤常规开展分子检测。该建议已纳入 ESMO 临床实践,推荐对转移性或复发性分泌性癌所有病例强制检测 NTRK 重排。指南还建议对其他复发性或转移性唾液腺恶性肿瘤开展综合性 NGS 检测,以识别潜在可靶向分子变异。尽管部分唾液腺肿瘤罕见,综合性分子检测对治疗选择与新治疗策略开发至关重要,尤其对复发性或转移性肿瘤患者。
SalvGlandDx v2 panel 覆盖 WHO 第 5 版头颈部肿瘤分类中描述的多数基因变异。然而,部分变异(如 IDH2 突变)尚未纳入 panel,其中 1 例纳入病例的最终分型需额外 DNA 测序。认识综合性 panel 的局限性对结果解读至关重要。且由于唾液腺肿瘤的分子(重新)分类仍在推进,日常应用的分子检测需同步更新。例如腺泡细胞癌中致癌转录因子 NR4A3 的基因间重排(“增强子劫持”)导致 RNA 过表达。由于位于基因间区,综合性 RNA 测序无法检出该重排。意识到这一点后,可检出后续 RNA 过表达并用于诊断。因此,与临床分子生物学家密切合作对 RNA 测序结果解读至关重要。
本研究存在若干局限性。首先,本院并非对所有唾液腺肿瘤常规开展 RNA 测序,存在选择偏倚风险。然而,鉴于队列涵盖多数唾液腺肿瘤(良性 35%、恶性 48%),且结果以描述性为主,研究者认为分析稳健。同样值得注意的是,在 SalvGlandDx v2 panel 推广与评估期间,本院对 RNA 测序的应用阈值普遍较低。较低的应用阈值有助于熟悉诊断检出率及用于教学场景,预计随着经验积累未来 RNA 测序应用会减少。该实践可能增加形态特征典型、评分为 1A 的病例比例,但也提高了队列的普遍适用性。其次,采用评分体系系统性评估 RNA 测序的贡献。尽管该方法为量化诊断价值提供结构化框架,但也可能无法捕捉多学科讨论中个体病例诊断过程的细微差异。评分采用保守方式,当仅通过(专家)复阅 H&E 与 IHC 即可得出最终分型时,将 RNA 测序结果归为无诊断价值(评分 3)。通过该方法,SalvGlandDx v2 panel 的诊断影响未被高估。最后,SalvGlandDx v2 panel 验证显示 RNA 与 DNA 测序在检出激活热点突变时一致性极佳。然而,仅基于 RNA 方法的突变检测可能遗漏大型肿瘤抑制基因(如 TP53)中的特定变异。
基于这些结果与既往文献,研究者建议在经充分 H&E 评估与现有 IHC 检测后,对形态特征不典型或重叠、复发性和 / 或转移性、以及良恶性鉴别诊断广泛的肿瘤考虑 RNA 测序。此外,切除前按 Milan 分类为 IVb 的细针穿刺标本,若细胞学尚未开展综合性分子分析,部分病例可从中获益。
本研究证实采用 SalvGlandDx v2 panel 进行综合性 RNA 测序在常规诊断实践中的诊断价值。该检测是阶梯式诊断策略中重要的最终环节,可确认诊断、细化鉴别诊断并识别潜在治疗靶点。后续临床管理可根据最终肿瘤分型进行调整,而分子分析已成为部分病例中至关重要的组成部分。
参考文献:
Burghout, Kimberly S T et al. “Molecular Analysis in Salivary Gland Tumors: Exploring the Diagnostic and Clinical Impact of Comprehensive Next Generation RNA Sequencing ("SalvGlandDx v2").” Head and neck pathology vol. 20,1 2. 22 Dec. 2025, doi:10.1007/s12105-025-01868-x


