全新递送策略,登上Nature大子刊!
时间:2026-05-08 20:37:10 热度:37.1℃ 作者:网络
深度解析医学证据,lxfs.net为你支撑决策
近年来,mRNA疫苗在肿瘤治疗和传染病防控中展现出巨大潜力,但其临床应用仍面临一个关键难题:如何让疫苗精准进入淋巴结这一免疫反应的“核心中枢”。现实中,大多数mRNA疫苗在体内会优先分布到肝脏等非靶器官,不仅降低了免疫激活效率,还可能带来系统性毒性风险。这种“跑偏”现象成为限制mRNA癌症疫苗疗效的重要瓶颈。
针对这一挑战,苏州大学钟志远教授、徐聪聪教授和周芳芳教授提出了一种全新的递送策略:利用单核细胞作为“天然运输工具”,将mRNA疫苗主动“送达”淋巴结。他们设计了一种名为TRAP的聚合物递送系统,通过与单核细胞表面的转铁蛋白受体结合,实现疫苗的高效转运。实验结果表明,这一系统不仅能显著提高淋巴结中的mRNA表达,还能激活强烈的抗肿瘤免疫反应,在多种动物模型中有效抑制肿瘤进展,并展现出良好的安全性和广泛适用性。相关成果以“Polymer–mRNA complexes for monocyte-trafficked, lymph node-targeted cancer vaccination”为题发表在《Nature Biomedical Engineering》上,Qiongzhe Ren, Xiaofei Zhao, Lili Zhou为共同第一作者。

研究团队首先从“找对靶点”入手。通过分析不同免疫细胞的基因表达,他们发现转铁蛋白受体TfR1在单核细胞中的表达水平显著高于其他细胞类型(图1a),这意味着单核细胞天然具备被精准“识别”的可能。进一步的分子动力学模拟揭示,TfR1表面存在暴露的半胱氨酸结构位点(图1b,c),为后续的化学结合提供了条件。基于这一结构特征,研究人员设计了一种带有环状二硫键的聚合物TRAP,使其既能牢固包裹mRNA,又能通过硫醇交换与TfR1结合,从而增强对单核细胞的靶向能力(图1f)。从物理性质来看,这种纳米颗粒直径约为60–70纳米(图1g),不仅尺寸适中,而且稳定性良好,适合体内递送。更重要的是,它在细胞内表现出优异的“逃逸能力”:相比传统材料容易被困在溶酶体中,TRAP能够有效释放mRNA进入细胞质,从而提高蛋白表达效率(图1j–m)。
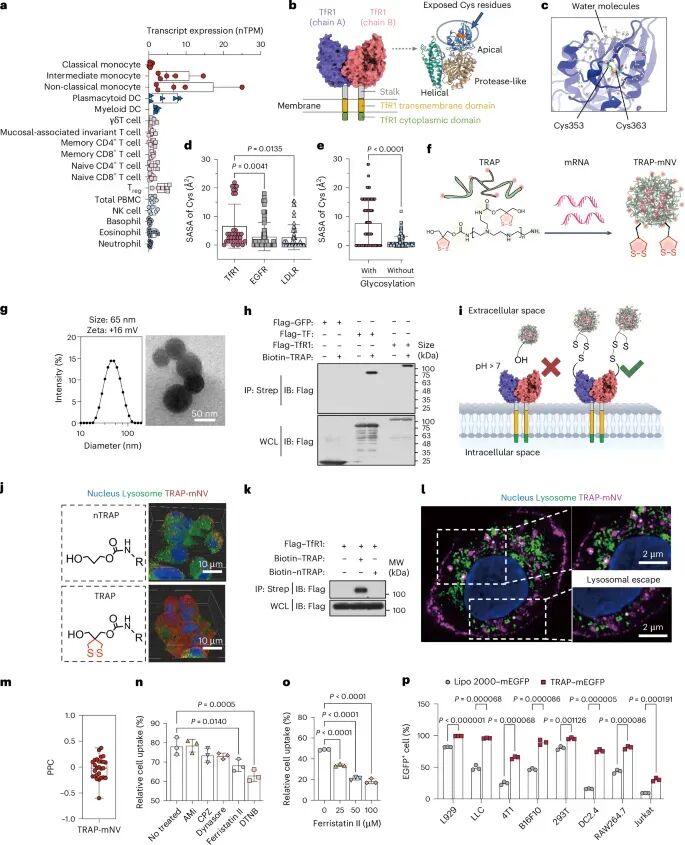
图1:TRAP纳米颗粒的设计原理及其与TfR1结合机制
当这一系统进入体内后,其“精准投递”能力开始显现。通过小鼠实验可以看到,在皮下注射后,mRNA几乎只在淋巴结中表达,而在肝脏、脾脏等主要器官中几乎检测不到明显信号(图2a–d)。更直观的数据表明,淋巴结与肝脏的表达比值高达40以上(图2i),远远优于传统脂质纳米颗粒。与此同时,荧光成像显示这些纳米颗粒在淋巴结中持续存在长达12小时以上(图2g,h),说明其靶向效果不仅精准,而且稳定。进一步分析发现,单核细胞在这一过程中扮演了关键角色:约95%的单核细胞摄取了TRAP纳米颗粒(图2n),并在24至36小时内持续携带这些“疫苗货物”(图2o)。显微图像中可以清晰看到,单核细胞与纳米颗粒在淋巴结中高度共定位(图2j,k),仿佛一支“运输队”将疫苗源源不断送入免疫中枢。
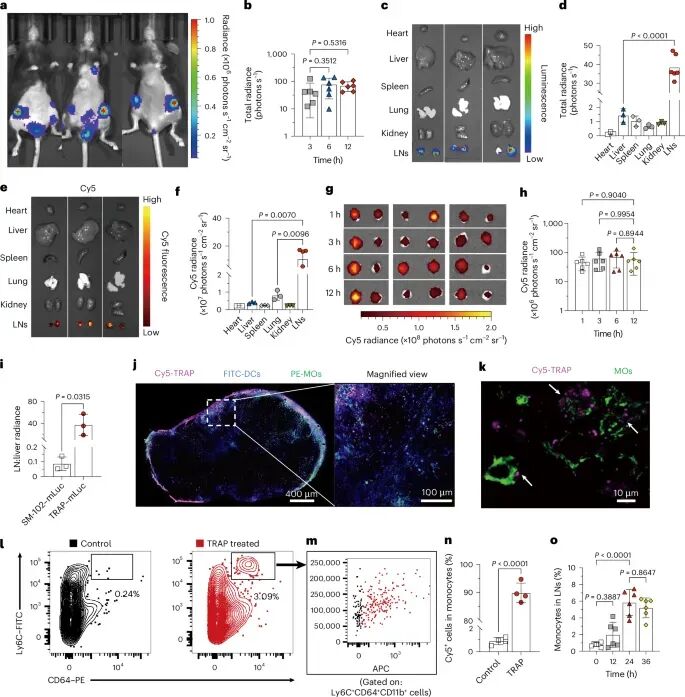
图2:TRAP介导的mRNA在体内主要富集于淋巴结
这种运输并非偶然,而是由免疫系统主动驱动的过程。研究发现,TRAP在注射部位会迅速引发类似炎症的反应,吸引大量单核细胞聚集(图3b–e)。这一过程与STING信号通路密切相关:TRAP能够诱导细胞释放线粒体DNA,从而激活cGAS–STING通路(图3k–n),引发先天免疫反应。随着炎症信号的增强,单核细胞不仅数量增加,而且更容易摄取纳米颗粒(图3f)。与此同时,树突状细胞的成熟标志物显著上调(图3g,h),抗原呈递能力增强(图3i,j),说明TRAP不仅是一个递送工具,还具备类似免疫佐剂的功能,能够放大免疫反应。
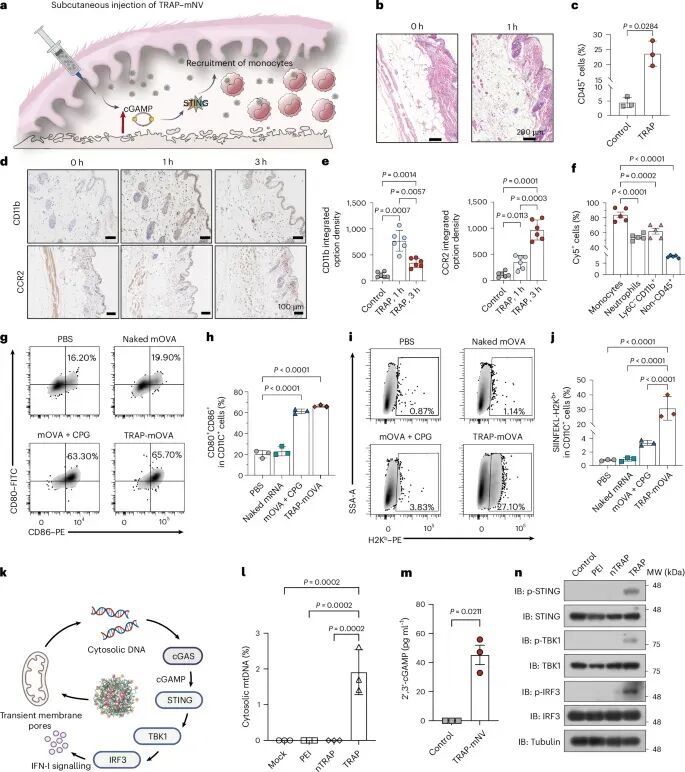
图3:TRAP激活STING通路并招募炎症性单核细胞
那么,这些携带疫苗的单核细胞是如何进入淋巴结的呢?研究进一步揭示,它们主要通过高内皮微静脉这一特殊血管结构进入(图4a)。体内实时成像显示,TRAP纳米颗粒在血管中随单核细胞迁移(图4b,c),并最终进入淋巴结。通过三维重建可以看到,这些颗粒在血管中分布均匀(图4e),随后进入淋巴组织。当研究人员用抗体阻断关键黏附分子PSGL-1或CD62L时,单核细胞进入淋巴结的能力显著下降(图4f–i),进一步证明这一“运输通道”的存在。这一机制就像为疫苗开辟了一条专属“高速公路”,确保其快速抵达目标位置。
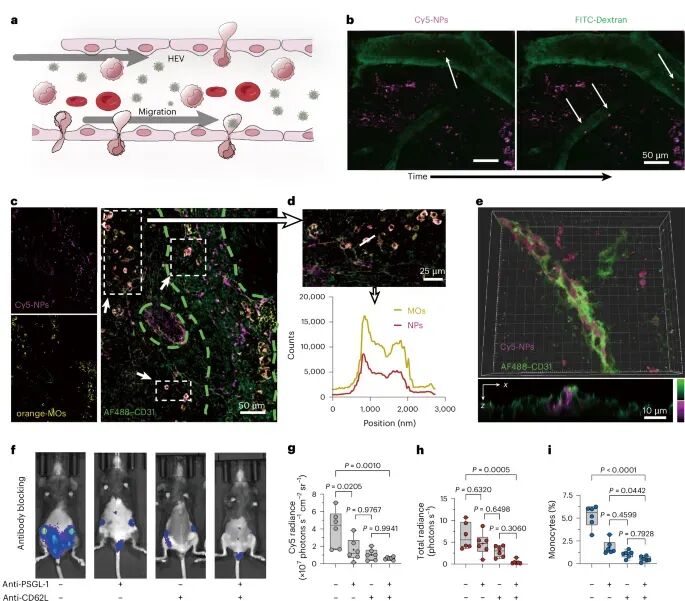
图4:单核细胞通过血管进入淋巴结的运输路径
更令人惊喜的是,这些单核细胞在完成运输任务后,并不会“功成身退”,而是继续参与免疫反应。研究发现,在淋巴结中,这些细胞逐渐表达CD11c和MHC-I等分子(图5c,d),表现出向树突状细胞分化的趋势,具备抗原呈递能力。换句话说,它们从“搬运工”转变为“指挥官”,直接参与激活T细胞。当研究团队进一步引入IL-12 mRNA进行联合递送时,这一过程被显著放大:IFN-γ等关键细胞因子水平明显升高(图5e,f),CD8+ T细胞和NK细胞的活性增强(图5k,l),抗原特异性T细胞数量显著增加(图5m,n)。ELISpot实验也证实,体内产生了大量分泌IFN-γ的免疫细胞(图5o),说明这一策略能够有效激活适应性免疫系统。
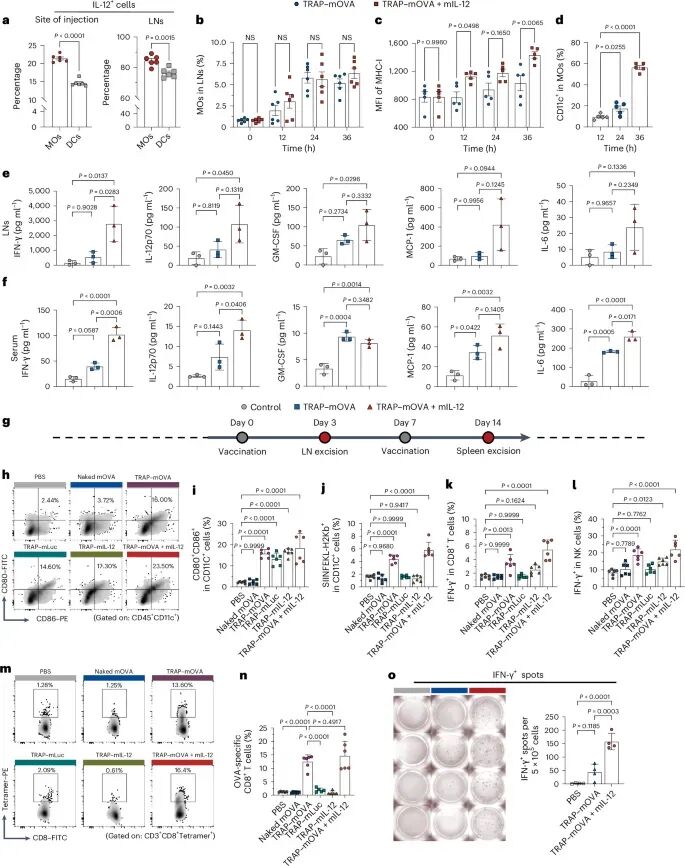
图5:单核细胞分化并激活T细胞免疫反应
在肿瘤治疗方面,这种免疫增强效果转化为显著的抗癌能力。在黑色素瘤模型中,TRAP递送的mRNA疫苗能够明显抑制肿瘤生长(图6f–h)。当与抗PD-1免疫治疗联合使用时,疗效进一步提升,部分小鼠实现完全缓解(图6i)。更重要的是,这种策略不仅作用于注射部位的肿瘤,还能抑制远端肿瘤生长,说明其诱导了系统性免疫反应。在转移模型中,疫苗同样显著延长了生存时间(图6k,l)。此外,在HPV相关肿瘤模型中,TRAP系统同样表现出良好的治疗效果(图7b),并诱导强烈的CD8+ T细胞反应和免疫记忆(图7c–g),进一步证明其广泛适用性。
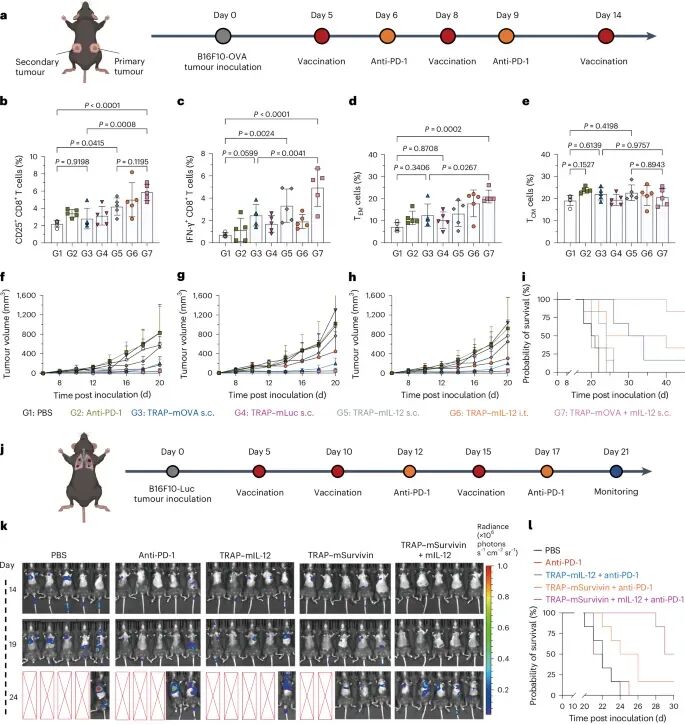
图6:TRAP疫苗在黑色素瘤模型中的抗肿瘤效果
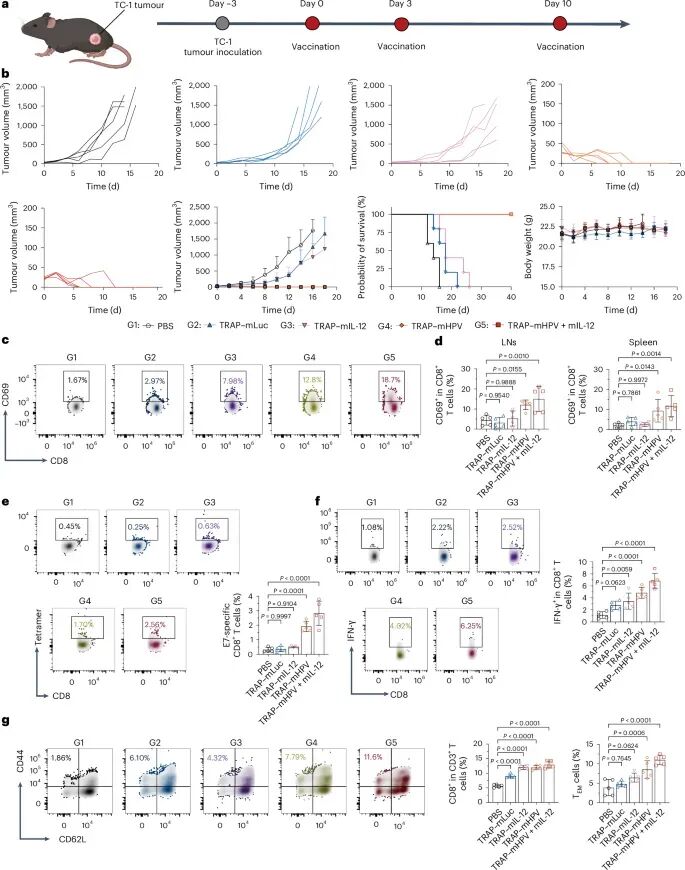
图7:TRAP疫苗在HPV肿瘤模型中的免疫与治疗表现
小结
总体来看,这项研究提出了一种全新的mRNA疫苗递送思路:通过单核细胞实现对淋巴结的精准靶向,不仅解决了传统疫苗“分布不准”的问题,还同时增强了免疫激活能力。该系统兼具递送与免疫调控双重功能,在多种肿瘤模型中展现出强大的抗癌潜力。未来,随着材料进一步优化以及在人类中的验证推进,这一策略有望成为下一代癌症疫苗的重要方向,为精准免疫治疗带来新的突破。
原文链接:
https://www.nature.com/articles/s41551-026-01672-0


