【绘真科普】基因检测如何辅助心脑血管疾病患者精准用药?
时间:2026-05-08 20:02:46 热度:37.1℃ 作者:网络
心脑血管疾病是一组以心脏和血管为主要病变部位的疾病统称,主要包括冠心病、高血压、动脉粥样硬化等。抗血小板药物、他汀类药物、降压药等药物可以减轻患者症状、延缓疾病进展以及改善预后。然而,不同患者对上述药物的治疗效果存在较大的个体差异。
药物基因组学(Pharmcogenomics,PGx)描述了基因组改变在药物反应中的作用,与药代动力学和药效学特性相关。心血管疾病患者进行PGx检测,可以给予医师用药方面的参考,从而制定精准的治疗方案,提高药物疗效和(或)降低药物毒性。基于指南共识以及PharmGKB等权威数据库中基因多态性与药物的疗效或毒副作用关系证据,我司推荐了心血管疾病个体化用药基因检测系列项目,可以辅助临床综合基因型、证据等级以及诊疗规范推荐用药等信息,决策适宜的治疗方案。
一、基因多态性检测与抗血小板用药建议
抗血小板药物可抗血小板的黏附和聚集,防止血栓形成,有助于防止血管阻塞性病变的病情发展,用于预防冠心病及脑动脉血栓栓塞。对于急性冠状动脉综合征和接受经皮冠状动态介入治疗的患者,通常推荐包括阿司匹林和P2Y12受体拮抗剂在内的双重抗血小板治疗。P2Y12受体拮抗剂包括氯吡格雷、普拉格雷和替格瑞洛。
氯吡格雷是一种前体药,需要通过连续两个依赖CYP2C19酶的步骤转化为活性产物,发挥抗血小板效应。而CYP2C19基因多态性可导致酶活性的个体化差异,使人群出现超快速代谢者(UM)、快代谢者(RM)、中间代谢者(IM)和慢代谢者(PM)4种异常表型。CYP2C19*`1为野生型,正常代谢者(NM)的基因型为CYP2C19*1/*1。CYP2C19*2(rs4244285,c.681G>A)导致剪接缺失变异,GYP2C19*3(rs4986893,c.636G>A)为终止密码子突变,这2种基因型都会导致CYP2C19酶缺陷。IM携带CYP2C19*2或者CYP2C19*2杂合子基因型,而PM则携带CYP2C19*2/*2、CYP2C19*2/*3或者CYP2C19*3/*3基因型。CYP2C19*17(rs12248560,-806C>T)能够增强酶活性,RM携带CYP2C19*1/*17基因型,UM则携带CYP2C19*17/*17基因型[1]。
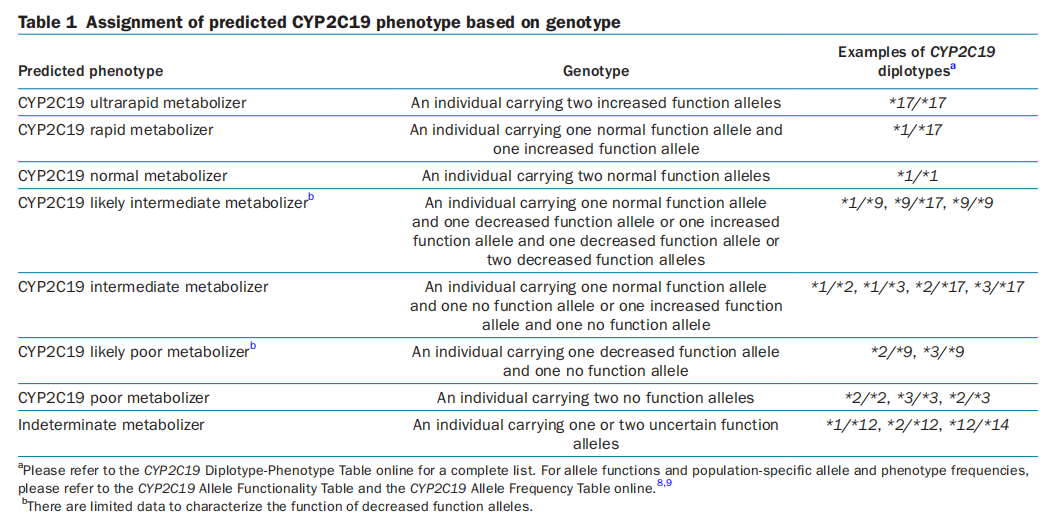
图1 基于CYP2C19的基因型预测其不同代谢表型类别
《药物代谢酶和药物作用靶点基因检测技术指南(试行)》(以下简称“指南”)推荐,增加PM基因型个体氯吡格雷的剂量,或选用其他不经CYP2C19代谢的抗血小板药物如替格瑞洛等[2]。2022年更新的《CPIC氯吡格雷指南》建议,UM和RM表型患者,考虑使用标准剂量(75mg/天)氯吡格雷治疗,且与较高的出血风险无关联。NM表型患者,使用标准剂量氯吡格雷治疗,IM和PM表型患者,尽量避免使用氯吡格雷治疗,如无禁忌症,可按标准剂量使用普拉格雷或替格瑞洛治疗[1]。
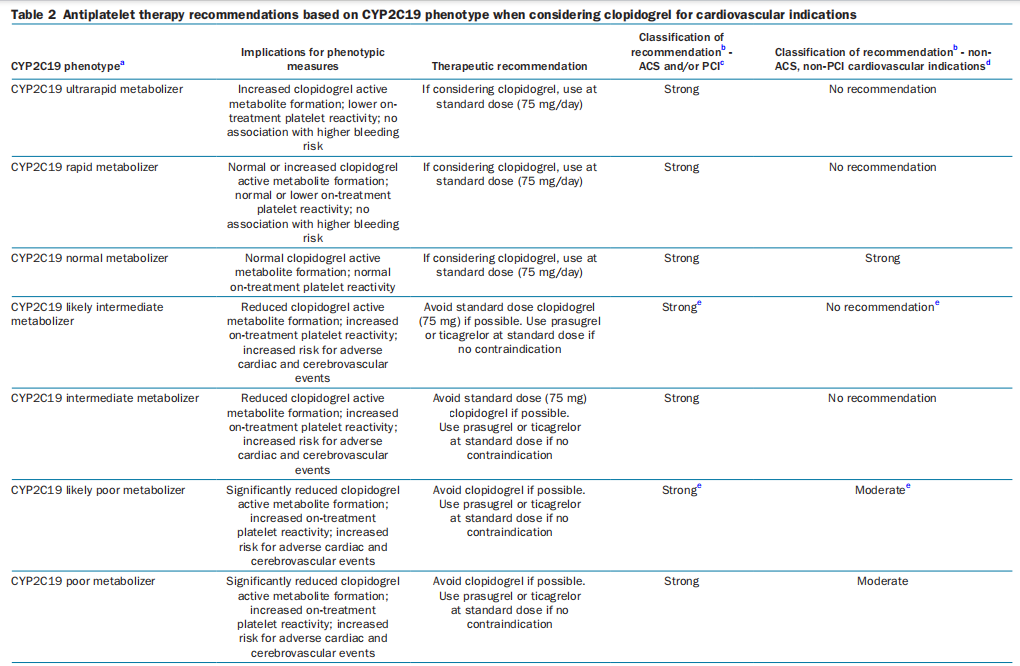
图2 CYP2C19表型与抗血小板治疗氯吡格雷用药推荐
《药物基因组学在现代心血管疾病治疗中的作用:欧洲心脏学会心血管药物治疗工作组的一项立场声明》(以下简称“欧洲声明”)推荐,对于根据基因分型判定为IM或PM患者,应避免使用氯吡格雷。如有条件,在对高危心血管疾病(血栓形成或出血高危)患者处方氯吡格雷之前,应考虑进行基因分型,尤其对预防直接植入术后血栓形成[3]。

图3 欧洲心脏学会心血管药物治疗工作组推荐CYP2C19基因分型检测辅助氯吡格雷用药
二、基因多态性检测与抗凝血用药建议
香豆素类药物可通过抑制维生素K环氧化物还原酶复合体亚单位1(VKORC1),导致凝血因子II、VII、IX和X的功能降低,可用于预防或治疗血栓栓塞。 华法林是常见的香豆素类药物,其临床疗效和不良反应存在很大的个体差异。该药物稳定剂量范围的低限和高限之间至少相差25倍(0.16-15.5mg/d),其中约55%-60%主要源于VKORC1基因变异(约25%)和CYP2C9基因变异(约15%),其他原因包括CYP4F2基因变异(约1%-7%)和临床因素(如年龄、体质指数、吸烟等)。
VKORC1基因编码的维生素k氧化还原酶是华法林的作用靶点,其基因变异可通过影响VKORC1酶表达,从而影响华法林的敏感性。VKORC1基因启动子区(rs9923231,-1639G>A)变异可影响VKORC1的表达,是导致华法林用药剂量个体差异的主要原因之一。与该位点AA基因型患者相比,GA基因型和GG基因型患者的平均华法林剂量分别增加52%和102%。CYP2C9是细胞色素P450酶(CYP)第二亚家族中的重要成员,是S-华法林对映体的主要代谢酶。
CYP2C9*2(rs1799853,c.430C>T)和CYP2C9*3(rs1057910,c.1075A>C)均导致CYP2C9酶活性降低,CYP2C9*3纯合子个体酶活性仅为该位点野生型纯合子基因型个体(CYP2C9*1)的4%-6%。CYP4F2基因编码维生素K单氧酶,参与维生素K代谢,从而影响华法林对VKORC1酶的抑制作用。CYP4F2*3(rs2108622,c.1297G>A)可导致酶活性降低,CYP4F2*1野生型纯合子基因型个体代谢活性最高,CYP4F2*3杂合子其次,CYP4F2*3纯合子活性最低。CYP4F2*3纯合子个体酶活性下降导致维生素K浓度升高,华法林抗凝效果大幅减弱。
指南推荐,根据VKORC1和CYP2C9的联合基因型建议华法林初始用药剂量。欧洲声明指出,建议在开始华法林治疗前,进行前瞻性基因分型。如已获取基因型信息,应将其用于指导华法林起始治疗剂量。VKORC1基因-1639G>A变异,需减低华法林剂量,CYP2C9基因型(*2,*3等),也需减低华法林剂量,而CYP4F2*3需增高华法林剂量。
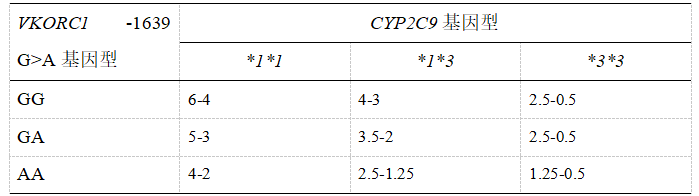
图4 指南推荐根据VKORC1和CYP2C9联合基因型建议华法林初始用药剂量

图5 欧洲声明推荐基因型与华法林剂量需求
苯丙香豆素和醋硝香豆素,也属于香豆素类抗凝血药物,作用于VKORC1靶点。VKORC1基因启动子区(rs9923231,-1639G>A)和内含子区(rs9934438,c.1173C>T)变异,均会导致VKORC1酶活性降低,需要降低苯丙香豆素和醋硝香豆素的使用剂量。另外,CYP2C9参与醋硝香豆素代谢,其*2(rs1799853,c.430C>T)和*3(rs1057910,c.1075A>C)均导致CYP2C9酶活性降低,需要降低醋硝香豆素剂量。
三、基因多态性检测与降血压用药建议
高血压是导致心血管疾病发病和死亡风险增加的首要危险因素。β受体阻滞剂,主要通过抑制过度激活的交感神经活性、抑制心肌收缩力、减慢心率发挥降压作用。美托洛尔、卡维地洛和普莱洛尔等一些β受体阻滞剂经CYP2D6代谢,其中美托洛尔的消除对CYP2D6依赖程度最高,口服剂量的70%-80%需经CYP2D6介导的生物转化。其他β受体阻滞剂(如阿替洛尔和比索洛尔)不经CYP2D6代谢或经其代谢的程度微不足道。
目前,已经发现CYP2D6基因的多种遗传变异,不同变异类型对酶活性和药物代谢的影响不一[4]。根据CYP2D6的活性,将人群分为超快代谢(UM)、正常代谢(NM)、中间代谢(IM)和慢代谢(PM)共4种表型。CYP2D6(rs1065852,c.100C>T)变异是亚洲人群最常见的突变位点,会导致酶活性降低。该变异包括在*4、*10、*36、*37等多个基因型中,但对于*10来讲,是关键变异。根据CPIC和DPWG共识,CYP2D6*1/*1和CYP2D6*1/*10为NM,而CYP2D6*10/*10为IM[5]。
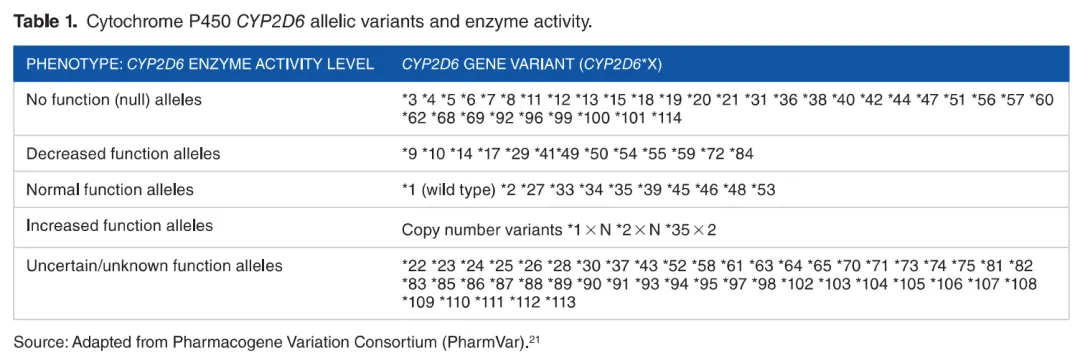
图6 CYP2D6等位基因变异与酶活性
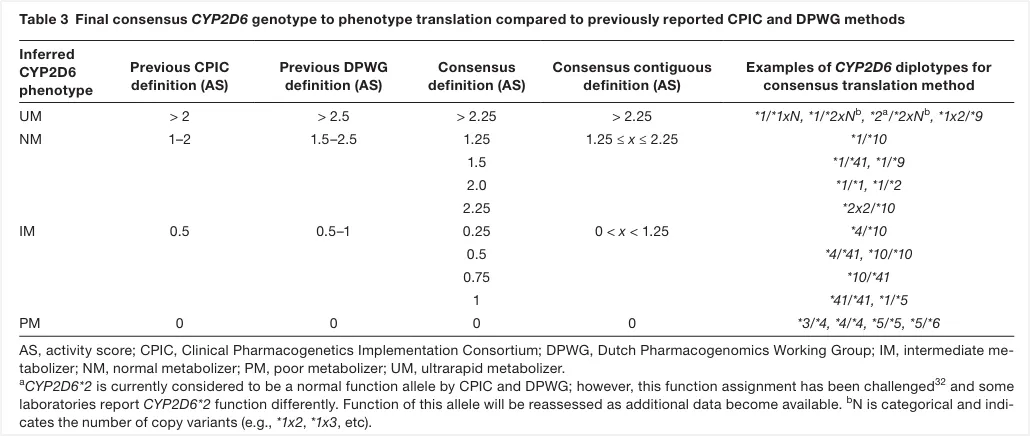
图7 CYP2D6基因型转换为表型的最终共识
血管紧张素转化酶抑制剂(ACEI)是通过抑制血管紧张素转换酶(ACE)而发挥降压作用。作为ACEI的靶点,其编码基因ACE位于17号染色体17q23,第16号内含子区存在288bp的Alu插入(Insertion)/缺失(Deletion)多态性,导致3种基因型:II(插入纯合子)、ID(插入缺失杂合子)和DD(缺失纯合子)。ACEI/D多态性可影响血浆ACE的水平,DD基因型个体血浆ACE的活性升高,依那普利治疗后ACE活性下降更明显。在初治的高血压患者中,DD基因型患者福辛普利的降压疗效增强。为取得最佳疗效,指南建议临床上在选择ACEI类药物进行治疗前对ACE I/D多态性进行检测,以指导选择合适的ACEI类药物。
四、基因多态性检测与降血脂用药建议
低密度脂蛋白胆固醇(LDL-C)是动脉粥样硬化性心血管疾病(ASCVD)的致病性危险因素。他汀类药物是目前临床应用最为广泛的调脂药,通过竞争性抑制HMG-CoA还原酶,从而抑制细胞内胆固醇的合成,降低血液中总胆固醇(TC)及LDL-C。然而,其不良反应及疗效具有个体化差异。
《SLCO1B1和ApoE基因多态性检测与他汀类药物临床应用专家共识》指出,基因单核苷酸多态性(SNP)是导致他汀类药物个体化差异的重要原因,包括SLCO1B1、ApoE、ABCB1、ABCG2等。其中,证据相对充足且对他汀类药物的不良反应和疗效影响明确的基因主要是SLCO1B1和ApoE[6]。
SLCO1B1基因2个位点(c.388A>G,c.521T>C)的SNP会导致患者服用他汀类药物可增加发生不良反应的风险。这2个位点可形成4种单倍型:SLCO1B1*1a(388A-521T),SLCO1B1*1b(388G-521T),SLCO1B1*5(388A-521C),SLCO1B1*15(388G-521C)。其中,*1a和*1b的功能正常,不会影响SLCO1B1编码的OATP1B1转运功能,而*5和*15则会使OATP1B1的转运功能降低,致使他汀类药物血药浓度升高,增加肝转氨酶异常、肌病甚至横纹肌溶解症等不良反应的发生风险。
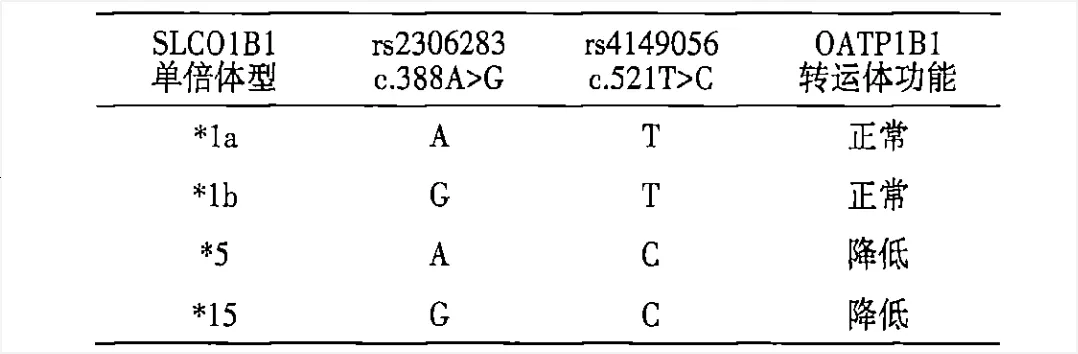
图8 SLCO1B1基因单倍体及其功能

图9 SLCO1B1基因型及其临床意义
ApoE基因2个位点(388T>C,526C>T)的SNP影响他汀类药物的调脂疗效,2个位点可形成3种单倍体型:ApoE2(388T-526T)、ApoE3(388T-526C)和ApoE4(388C-526C)。ApoE E2对低密度脂蛋白受体(LDL-R)亲和力下降,使用他汀类药物治疗时血TC和LDL-C降幅更大,降脂疗效较佳。而ApoE E4与LDL-R亲和力最高,ApoE E4携带者血脂水平更高,服用他汀类药物往往疗效不佳或无效。
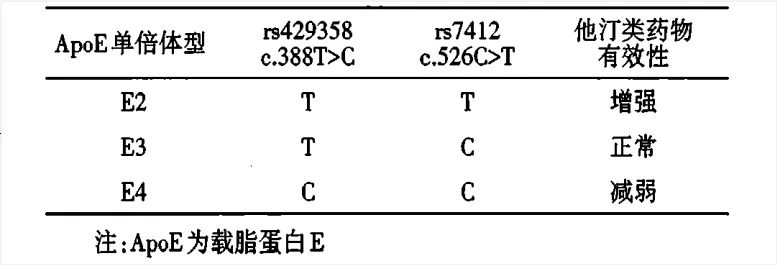
图10 ApoE单倍体型与他汀类药物有效性

图11 ApoE基因型及其临床意义
专家共识推荐,SLCO1B1*5及*15单倍体型携带者,在选择高强度及中等强度他汀类药物时,应依据基因型选择更适合的他汀类药物种类和剂量。若同时合并ApoE E4单倍体型携带者,建议选择他汀类药物联合其他类降脂药,或其他降脂方案,以达到更好的治疗效果。
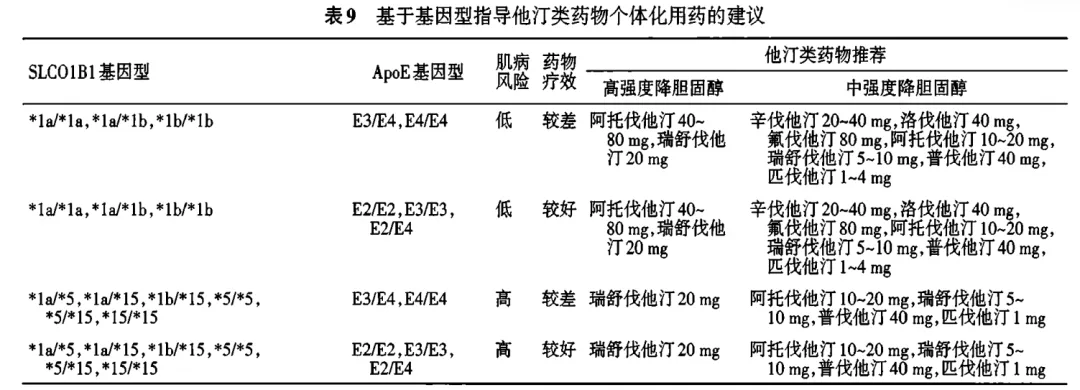
图12 基于基因型指导他汀类药物个体化用药的建议
五、基因多态性检测与降血糖、抗痛风、抗心律失常及抗心绞痛用药建议
高血糖是引发心血管疾病的重要危险因素。患者通过口服双胍类(二甲双胍)、磺脲类药物(格列奇特、格列美脲、格列吡嗪等)、格列奈类(瑞格列奈、那格列奈、米格列奈)等降糖药物治疗,控制血糖升高。然而,药物的疗效或不良反应存在明显的个体化差异。已经有多项研究表明,基因多态性与之相关。以广泛使用的二甲双胍为例。研究表明,C11orf65(rs11212617,c.175-528G>T)的基因多态性与二甲双胍的临床疗效相关。二甲双胍治疗后,携带C11orf65 G等位基因的患者对空腹血糖的作用更好,GG基因型比TG基因型对糖化血红蛋白(HbA1c)的作用更好,C11orf65携带G等位基因比未携带者的胰岛素抵抗指数(HOMA-IR)降低的更多[7]。
高尿酸血症是由嘌呤代谢紊乱和(或)尿酸排泄减少引起的常见慢性病。长期高水平的血尿酸不仅可引发痛风、肾结石及肾功能损害,还与心血管疾病的发生发展密切相关。别嘌醇是痛风患者药物降尿酸治疗的主要药物。指南指出,HLA-B*5801等位基因与别嘌醇所致Stevens-Johnson综合征/中毒性表皮坏死松解症(SJS/TEN)相关。基于HLA-B*5801相关的2个位点(位点1:g.31312326T>G,位点2:g.32257337A>G)多态性检测,辅助HLA-B*5801阴阳性判断,分为3种情况:①当位点1基因型为TT时,位点2无论什么基因型,HLA-B*5801均为阴性;②当位点1基因型为GG时,位点2为GG基因型,HLA-B*5801为阴性,位点2为AA或AG基因型,HLA-B*5801为阳性;③当位点1基因型为GT时,位点2为GG基因型,HLA-B*5801为阴性,位点2为AA或AG基因型,HLA-B*5801为阳性。需要说明的是,第三种情况,位点1是GT杂合时,位点2是AG基因型,HLA-B*5801有50%概率是阳性,50%是阴性,考虑到不良反应后果比较严重,也判读为HLA-B*5801阳性。《高危高尿酸血症药物降尿酸治疗专家共识(2025版)》指出,别嘌醇治疗前应尽可能筛查HLA-B*5801基因,阳性者禁用[8]。
心律失常是常见的心血管疾病。氟卡尼、普罗帕酮、苯丙英钠等药物可用于抗心律失常治疗。研究表明,CYP2D6酶参与氟卡尼和普罗帕酮的代谢,CYP2D6基因(rs1065852,c.100C>T)多态性与不良反应相关。指南指出,CYP2C9酶参与苯丙英纳代谢,CYP2C9*2(rs1799853,c.430C>T)和CYP2C9*3(rs1057910,c.1075A>C)与不良反应相关。
心绞痛是由于冠状动脉供血不足,心肌急剧的、暂时的缺血与缺氧所引起的临床综合征。硝酸甘油可以缓解和预防心绞痛急性发作。指南指出,ALDH2酶参与硝酸甘油的代谢,其编码基因ALDH2具有多态性,携带ALDH2*2(rs671,c.1510G>A)变异的个体酶活性下降,杂合子为野生型的10%,纯合子酶活性缺失。携带ALDH2*2的心绞痛患者,代谢硝酸甘油能力下降,应尽可能改用其他急救药物,避免硝酸甘油含服无效。
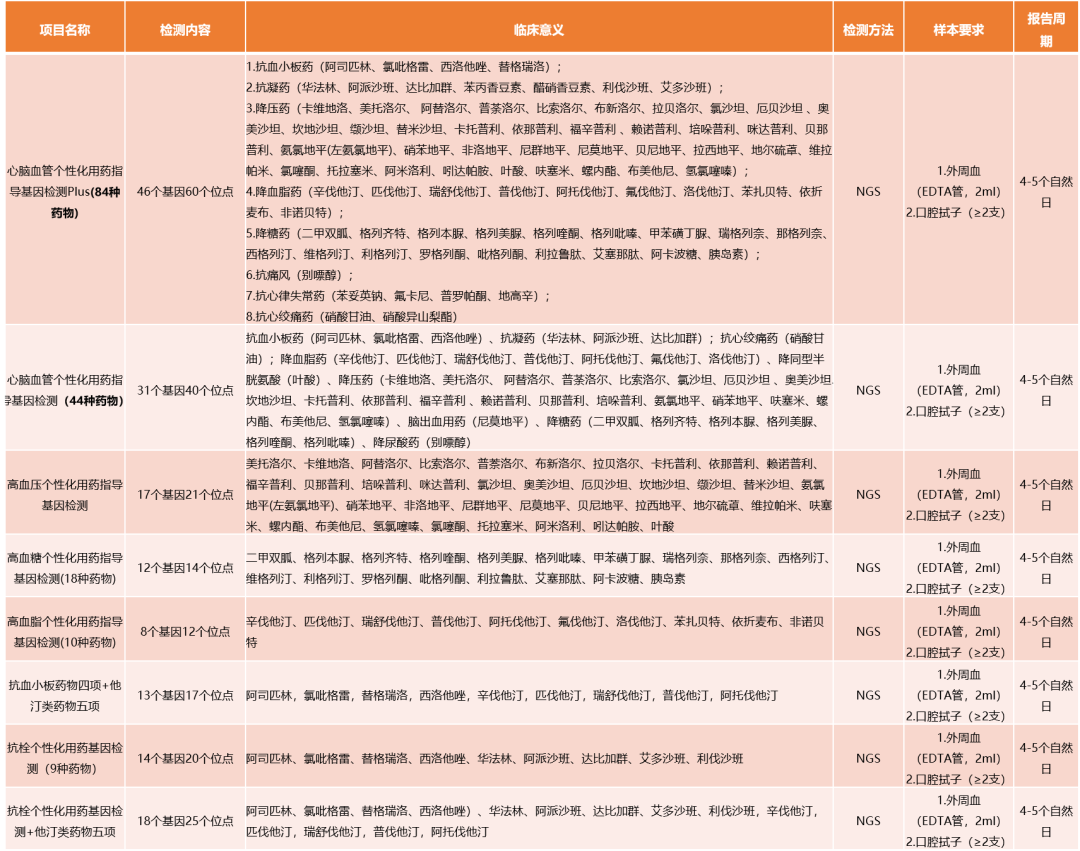
表1 心血管疾病个体化用药基因检测系列项目简介
参考文献:
[1]Lee CR, Luzum JA, Sangkuhl K, Gammal RS, Sabatine MS, Stein CM, Kisor DF, Limdi NA, Lee YM, Scott SA, Hulot JS, Roden DM, Gaedigk A, Caudle KE, Klein TE, Johnson JA, Shuldiner AR. Clinical Pharmacogenetics Implementation Consortium Guideline for CYP2C19 Genotype and Clopidogrel Therapy: 2022 Update. Clin Pharmacol Ther. 2022 Nov;112(5):959-967. doi: 10.1002/cpt.2526. Epub 2022 Feb 8. PMID: 35034351; PMCID: PMC9287492.
[2]中华人民共和国国家卫生和计划生育委员会. 药物代谢酶和药物作用靶点基因检测技术指南(试行)概要[J]. 实用器官移植电子杂志,2015,3(5):257-267.DOI:10.3969/j.issn.2095-5332.2015.05.001.
[3]Magavern EF, Kaski JC, Turner RM, Drexel H, Janmohamed A, Scourfield A, Burrage D, Floyd CN, Adeyeye E, Tamargo J, Lewis BS, Kjeldsen KP, Niessner A, Wassmann S, Sulzgruber P, Borry P, Agewall S, Semb AG, Savarese G, Pirmohamed M, Caulfield MJ. The role of pharmacogenomics in contemporary cardiovascular therapy: a position statement from the European Society of Cardiology Working Group on Cardiovascular Pharmacotherapy. Eur Heart J Cardiovasc Pharmacother. 2022 Jan 5;8(1):85-99. doi: 10.1093/ehjcvp/pvab018. Erratum in: Eur Heart J Cardiovasc Pharmacother. 2022 Dec 15;9(1):116. doi: 10.1093/ehjcvp/pvac038. PMID: 33638977; PMCID: PMC12375811.
[4]Orrico KB. Basic Concepts in Genetics and Pharmacogenomics for Pharmacists. Drug Target Insights. 2019 Dec 3;13:1177392819886875. doi: 10.1177/1177392819886875. PMID: 31832012; PMCID: PMC6891005.
[5]Caudle KE, Sangkuhl K, Whirl-Carrillo M, Swen JJ, Haidar CE, Klein TE, Gammal RS, Relling MV, Scott SA, Hertz DL, Guchelaar HJ, Gaedigk A. Standardizing CYP2D6 Genotype to Phenotype Translation: Consensus Recommendations from the Clinical Pharmacogenetics Implementation Consortium and Dutch Pharmacogenetics Working Group. Clin Transl Sci. 2020 Jan;13(1):116-124. doi: 10.1111/cts.12692. Epub 2019 Oct 24. PMID: 31647186; PMCID: PMC6951851.
[6]中国中西医结合学会检验医学专业委员会,浙江省免疫学会临床免疫诊断专业委员会,浙江省药理学会治疗药物监测研究专业委员会. SLCO1B1和ApoE基因多态性检测与他汀类药物临床应用专家共识[J]. 中华检验医学杂志,2023,46(07):672-680.
[7]闵翼,许雄伟.C11orf65、SLC47A1基因多态性与二甲双胍临床疗效的相关性分析[J].中国医学创新, 2019.DOI:CNKI:SUN:ZYCX.0.2019-31-019.
[8]中华医学会风湿病学分会,中国初级卫生保健基金会风湿免疫专委会. 高危高尿酸血症药物降尿酸治疗专家共识(2025版)[J]. 中华医学杂志,2025,105(29):2469-2482.


